
分析 (1)一水合氨是弱碱,在水溶液能电离出氢氧根离子,导致氢氧根离子浓度大于氢离子浓度;
(2)氯化铵是强酸弱碱盐,能水解导致溶液中氢离子浓度大于氢氧根离子浓度;盐类水解反应是吸热反应,升高温度能促进水解;
(3)氨水是弱电解质,在水中电离程度很小;氯化铵是强酸弱碱盐,能水解但水解程度很小,主要以电离为主,据此分析铵根离子浓度大小.
解答 解:(1)一水合氨是弱碱,在水溶液能电离出氢氧根离子,导致氢氧根离子浓度大于氢离子浓度,溶液呈碱性,溶液的pH>7,电离方程式为:NH3•H2O?NH4++OH-,
故答案为:>;NH3•H2O?NH4++OH-;
(2)氯化铵是强酸弱碱盐,铵根离子能水解导致溶液中氢离子浓度大于氢氧根离子浓度,溶液呈酸性;盐类水解反应是吸热反应,升高温度平衡向正反应方向移动,所以能促进水解,
故答案为:酸;氯化铵是强酸弱碱盐,铵根离子能水解导致溶液中氢离子浓度大于氢氧根离子浓度,溶液呈酸性;促进;
(3)氨水是弱电解质,在水中电离程度很小;氯化铵是强酸弱碱盐,能水解但水解程度很小,主要以电离为主,所以相同浓度的氨水和氯化铵溶液,氯化铵溶液中铵根离子浓度较大,但都小于0.1mol/L,故选b,
故答案为:b.
点评 本题考查了弱电解质的电离,明确“盐类的水解是微弱的(弱酸弱碱盐除外),主要以电离为主”是解本题的关键,题目难度不大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(CN-)>c(H+)>c(OH-) | B. | c(HCN)+c(CN-)=0.04 mol•L-1 | ||
| C. | c(Na+)+c(H+)=c(CN-)+c(OH-) | D. | c(CN-)>c(HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 着色剂---胡萝卜素、苯甲酸钠 | B. | 调味剂---亚硝酸钠、味精 | ||
| C. | 防腐剂---氯化钠、柠檬黄 | D. | 营养强化剂---酱油中加铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
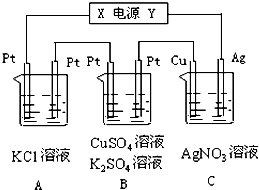 如图所示,若电解5min时铜电极质量增加2.16g,试回答:
如图所示,若电解5min时铜电极质量增加2.16g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素间形成的化学键都是共价键 | |
| B. | 第三周期主族元素的最高正化合价等于它所处的族序数 | |
| C. | 短周期元素形成离子后,最外层都达到8电子稳定结构 | |
| D. | 最外层电子数相同的原子属于同一族且化学性质相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
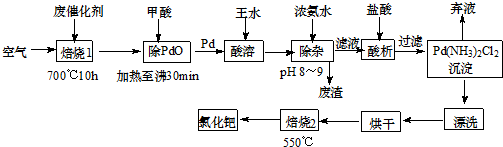
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com