
| A. | NaOH | B. | Na2CO3 | C. | Ca(OH)2 | D. | NaCl |
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA | |
| B. | pH=1的稀硫酸中含有的H+数为0.1NA | |
| C. | 133g氯化铝分子中含有铝离子的个数为NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO 32- NO3- SO42- SiO32- |
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2来中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干水和干冰是同一种物质 | |
| B. | 干水是纯净物 | |
| C. | 用干水吸收CO2有助于减缓温室效应 | |
| D. | 干水吸收CO2的过程只发生物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中可能含有K+,一定没有HCO3-和OH-,将产生的无色气体通入澄清石灰水中,澄清石灰水变浑浊 | |
| B. | 原溶液中一定含有Cl-和NO3-,可能含有SO42-,反应生成的无色气体遇空气变红棕色 | |
| C. | 原溶液中所含的阳离子为Mg2+、Fe2+,加入稀盐酸所发生的反应为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| D. | 若向原溶液中加入过量NaOH溶液,将所得沉淀过滤、洗涤、灼烧到恒重,得到的固体质量为107 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏时,当烧瓶中液体出现暴沸时,要立即添加碎瓷片 | |
| B. | 蒸发操作时,应使溶液蒸发至干,以保证得到的固体中没有任何水分 | |
| C. | 分液操作时,分液漏斗中下层液体先从下口放出,再让上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
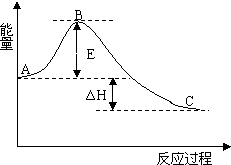 2SO2(g)+O2(g)=2SO3(g) 反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g) 反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com