
| A. | 胶粒直径在1~100nm之间 | B. | 胶粒作布朗运动 | ||
| C. | 胶粒通过吸附而带正电荷 | D. | 胶粒不能透过半透膜 |
分析 根据胶体中分散质的微粒大小为1-100nm,胶粒不能透过半透膜,胶粒时刻在不停的无规则运动,氢氧化铁胶粒带正电,因为都带同种电荷,胶粒之间是相排斥的,不易聚集成大颗粒,使氢氧化铁胶体可以稳定存在等知识点来解题.
解答 解:A.胶粒直径介于1nm-100nm之间,胶体微粒大小不是能稳定存在的主要原因,故A错误;
B.胶体中的粒子无时无刻不在做无规则运动,但不是胶体稳定存在的主要原因,故B错误;
C.胶体不带电,氢氧化铁胶粒带正电,因为都带同种电荷,胶粒之间是相排斥的,不易聚集成大颗粒,达不到100nm以上就沉不下来,故C正确;
D.胶粒不能透过半透膜,但是胶体微粒大小不是能稳定存在的主要原因,故D错误;
故选C.
点评 本题考查了胶体的一些性质,难度不大,如布朗运动,分散质的微粒大小为1-100nm,胶粒不能透过半透膜,胶体稳定存在原因带同种电荷,胶粒之间是相排斥的,不易聚集成大颗粒,不形成沉淀等知识点.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌是负极,氧化银是正极 | |
| B. | 锌发生还原反应,氧化银发生氧化反应 | |
| C. | 溶液中OH-向正极移动,K+、H+向负极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液的pH逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12L | B. | 3.36L | C. | 2.24L | D. | 4.48L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)
;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
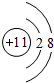 .
.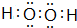 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
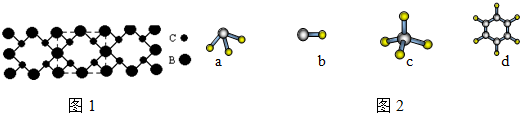

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com