
| 加料方式(mol) | H2的体积分数 | ||||
| 物质 | CO(g) | H2O(g) | CO2(g) | H2(g) | |
| 加料一 | 1 | 3 | 0 | 0 | a% |
| 加料二 | 0 | 1.2 | 0.6 | 0.6 | b% |
分析 (1)利用盖斯定律,根据已知热化学方程式乘以合适的系数进行相应加减构造目标热化学方程式,反应热也乘以相应的系数进行相应的加减,据此书写判断;
(2)①反应是放热反应升温平衡逆向进行,平衡常数减小;
②若要使上述反应开始时向正反应方向进行,浓度商小于平衡常数计算判断;
③将加料二的氢气、二氧化碳转化为CO和水,与加料一相比较,结合浓度对平衡移动的影响判断.
(3)①在氢氧燃料电池的正极上发生得电子的反应,氧气被还原生成氢氧根离子;
②电解硫酸铜时,阳极上是氢氧根放电,阴极上是铜离子放电,
电解硫酸铜时,阴极上是铜离子先放电,两极生成体积相同的气体,即阴极上:Cu2++2e-→Cu,2H++2e-→H2↑,当该电极上有1.28g Cu生成时,转移电子为$\frac{1.28g}{64g/mol}$×2=0.04mol,阳极上是氢氧根放电,即4OH-→O2↑+2H2O+4e-,当两极生成体积相同的气体时,则转移电子是一样的,所以共转移0.08mol电子,此时阴极上产生氢气是0.02mol,阳极上产生氧气是0.02mol,两极上生成标准状况下气体的体积为0.04mol×22.4L/mol=0.896L.
解答 解:(1)已知:①2CO(g)+O2(g)=2CO2(g)△H=-566kJ•moL-1
②2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ•moL-1
根据盖斯定律,①-②得2CO(g)+2H2O(g)=2H2(g)+2CO2(g)△H=-566kJ•moL-1-(-483.6KJ•moL-1)=-82.4KJ•moL-1.
即CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1.
故答案为:CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1;
(2)①CO(g)+H2O(g)?CO2(g)+H2(g);△H<0,在850℃时,平衡常数K=1,升温到950℃时,平衡常数随温度变化,反应是放热反应,升温平衡逆向进行,平衡常数减小,K<1;
故答案为:K<1;
②850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO、3.0mol H2O、1.0mol CO2 和x mol H2,若要使上述反应开始时向正反应方向进行,说明此时的浓度商小于平衡常数,
则Q=$\frac{1.0×x}{1.0×3.0}$<1,
得到x<3,
故答案为:x<3;
③CO(g)+H2O(g)?CO2(g)+H2(g)
一 1mol 3mol 0 0
二 0 1.2mol 0.6mol 0.6mol
可知二相当于0.6molCO、1.8molH2O,与一中n(CO):n(H2O)都是1:3,因反应前后气体的体积不变,则压强对平衡移动没有影响,所以达到相同平衡状态,则a=b,
故答案为:=;
(3)①在氢氧燃料电池的正极上发生得电子的反应,即O2+2H2O+4e-═4OH-,故答案为:O2+4e-+2H2O═4OH-;
②电解硫酸铜时,阳极上是氢氧根放电,阴极上是铜离子放电,
电解原理方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;
电解硫酸铜时,阴极上是铜离子先放电,两极生成体积相同的气体,即阴极上:Cu2++2e-→Cu,2H++2e-→H2↑,当该电极上有1.28g Cu生成时,转移电子为$\frac{1.28g}{64g/mol}$×2=0.04mol,阳极上是氢氧根放电,即4OH-→O2↑+2H2O+4e-,当两极生成体积相同的气体时,则转移电子是一样的,所以共转移0.08mol电子,此时阴极上产生氢气是0.02mol,阳极上产生氧气是0.02mol,两极上生成标准状况下气体的体积为0.04mol×22.4L/mol=0.896L,
故答案为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;0.08;0.896.
点评 本题综合考查学生热化学、盖斯定律的应用、燃料电池和电解池的工作原等知识,为高频考点,侧重于学生的分析、计算能力的考查,属于综合知识的考查题,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
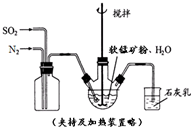 高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
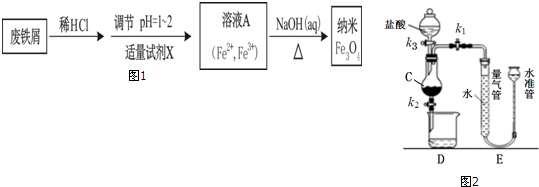
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入水时,溶液中c(OH-) 增大 | |
| B. | 加入少量NH4Cl固体,平衡向逆方向移动,电离平衡常数减小 | |
| C. | 通入少量HCl气体,溶液中c(NH4+)增大 | |
| D. | 降低温度,促进NH3•H2O电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③②④ | C. | ②①④③ | D. | ①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用FeCl2溶液吸收Cl2,选⑤ | B. | 分离Na2CO3溶液和油脂,选④ | ||
| C. | 用四氯化碳提取碘水中的碘,选③ | D. | 粗盐提纯,选①和② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com