
【题目】写出下列物质的名称:
A.(CH3)3CCH(CH3)(CH2)2CH(C2H5)2 A的名称是________;
B.(CH3)3CC≡CCH2CH3 B的名称是____;
C.![]() C的名称是_____
C的名称是_____
D.CH2OHCH(C2H5) CH2OH D的名称是________。
【答案】2,2,3-三甲基-6-乙基辛烷 2,2-二甲基-3-己炔 间二甲苯 2-乙基-1,3-丙二醇
【解析】
A中最长碳链有8个C,2、3号C上有甲基,6号C上有乙基;B中含碳碳三键的最长碳链有6个C,三键在3、4号C之间,且2号C上有甲基;C中苯环上1,3号碳上有甲基;D中含有羟基的最长碳链有3个碳原子,在1、3号C上含有羟基,在2号C上有乙基,结合系统命名法书写各物质的名称。
A.(CH3)3CCH(CH3)(CH2)2CH(C2H5)2中最长碳链有8个C,2、3号C上有甲基,6号C上有乙基,名称为2,2,3-三甲基-6-乙基辛烷;
B.(CH3)3CC≡CCH2CH3中含碳碳三键的最长碳链有6个C,三键在3、4号C之间,在2号C上有甲基,名称为2,2-二甲基-3-己炔;
C. 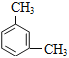 的名称为间二甲苯或1,3-二甲苯;
的名称为间二甲苯或1,3-二甲苯;
D.CH2OHCH(C2H5) CH2OH 中含有羟基的最长碳链有3个碳原子,在1、3号C上含有羟基,在2号C上有乙基,名称为2-乙基-1,3-丙二醇。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】某实验需要500mL0.10mol/L的Na2CO3溶液,现通过如下步骤配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水搅拌溶解;
②用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
③盖好瓶塞,反复上下颠倒,摇匀;
④把溶解固体后所得溶液冷却至室温,转入仪器A中;
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
(1)操作步骤的正确顺序为__(填序号)。
(2)称量的Na2CO3固体质量应为__g。
(3)仪器A的名称是__。
(4)取出100mL配制好的溶液,加蒸馏水稀释至c(Na2CO3)=0.02mol/L。则稀释后溶液的体积为__。
(5)下列关于容量瓶的使用方法中,正确的是__(填字母序号)。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.在烧杯中溶解固体后,迅速将溶液转移到容量瓶中
D.向容量瓶中转移溶液用玻璃棒引流
E.加水时水量超过了刻度线,迅速用胶头滴管将过量的水吸出
(6)下列操作会使所配溶液的物质的量浓度偏低的是__(填字母序号)。
A.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
B.定容读数时,俯视容量瓶上的刻度线
C.加水定容时,水量超过了刻度线
D.洗涤步骤中,洗涤液没有转入容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某抗酸药中碳酸钙固体的纯度(另一种成分为淀粉),称取12.5g此药片置于烧杯中,加入过量的稀盐酸,测得反应过程中烧杯和药品的总重量随时间的变化数据如下:
反应时间/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
烧杯和药品的总重/g | 310.0 | 306.8 | 305.9 | 305.7 | 305.6 | 305.6 | 305.6 |
计算:(1)共收集到标准状况下CO2的体积____________________;
(2)该样品中碳酸钙的质量分数________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把质量为mg的铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红而且质量仍为mg的是
A.NaOH溶液B.CH3COOHC.稀HNO3D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C 为短周期元素,它们的位置关系如图所示,已知 B、C 两元素原子核内质子数之和是 A 元素的原子核内质子数的 4 倍。

(1)写出 A、B 的元素符号:A____、B____。
(2)B 在周期表中的位置为____,C 的离子结构示意图为____。
(3)A 的氢化物的分子式为____;B、C 的最高价氧化物对应的水化物的分子式分别为____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
(1)CH3CH2CH2COOH________,
(2)HCOOC2H5________,
(3)CH3CH2CH2CH2Cl________,
(4)CH3CHO________,
(5)![]() _________,
_________,
(6)![]() _________,
_________,
(7)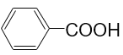 _________,
_________,
(8)CH3CH2CH=CHCH3_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)气态氟化氢中存在二聚分子(HF)2,这是由于__。
(2)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为__,中心I原子的杂化轨道类型为__。
(3)基态溴原子的电子排布式为__,碘原子价电子的电子排布图为__。
(4)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸点由高到低的顺序为__,I和Cl相比,电负性较大的是__,ICl中I元素的化合价为__。
(5)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为__(填序号)。
(6)卤化物RbICl2加热时会分解为晶格能相对较大的卤化物和卤素互化物,该反应的化学方程式为__。RbICl2的晶体结构与CsCl相似,晶胞边长为685.5pm,RbICl2晶胞中含有__个氯原子,RbICl2晶体的密度是__gcm-3(只要求列算式,不必计算出数值.阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为______________。
(2)反应前A的物质的量浓度是______________。
(3)10 s末,生成物D的浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取SO2并验证SO2的某些性质的装置(夹持装置和加热装置已略,气密性已检验),请回答下列问题:
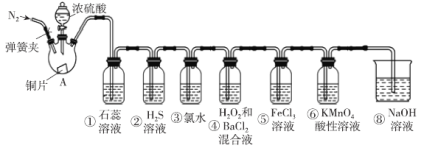
(1)在A中发生反应的化学方程式为___。
(2)①中的实验现象为紫色石蕊溶液___。
②中的实验现象为___,写出此化学反应方程式___。
③中的实验现象是___,写出此化学反应方程式___。
④中的实验现象是___,写出此化学反应方程式___。
⑤中的现象是溶液由黄色变为浅绿色,其反应的离子方程式为___。
(3)能体现出SO2还原性的实验序号是___。
(4)实验结束后需要通入N2,其目的是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com