
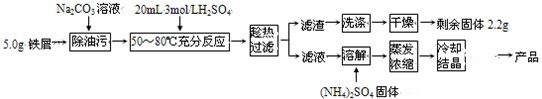
 (2009?广州模拟)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂,其实验室制备流程如下:
(2009?广州模拟)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂,其实验室制备流程如下: HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH- HCO3-+OH-,使Na2CO3溶液呈碱性,用显碱性的Na2CO3溶液洗去表面油污.
HCO3-+OH-,使Na2CO3溶液呈碱性,用显碱性的Na2CO3溶液洗去表面油污. HCO3-+OH-.
HCO3-+OH-.| 2.8g |
| 56g/mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com