
(14��)SO2 ��CO ��NOx �ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ƺ��������Ż��������滷������Ч;������ش��������⣺
��1����֪25�桢101kPaʱ��
2SO2(g) + O2(g)  2SO3(g) ��H1 = - 197 kJmol-1
2SO3(g) ��H1 = - 197 kJmol-1
H2O(g) = H2O(l) ��H2 = - 44 kJmol-1
2SO2(g) + O2(g) + 2H2O(g) = 2H2SO4(l) ��H3 = - 545 kJmol-1
��SO3(g)��H2O(l)��Ӧ���Ȼ�ѧ����ʽ�� ��
��2������Ӧ2H2��g��+ O2 ��g��=2H2O��g ��,��H=-241.8kJmol-1�������±�������x=______kJmol-1��
��ѧ�� | H-H | O�TO | O-H |
�Ͽ�1mol��ѧ�����������/kJ | 436 | x | 463 |
��3���״�����Ҳ��һ������Դ���ȼ�ϡ���ҵ�Ͽ���CO��H2��ȡ�״����Ȼ�ѧ����ʽΪ��CO(g)+2H2(g) CH3OH(g) ��H=-90 kJmol-1
CH3OH(g) ��H=-90 kJmol-1
�ٸ��¶��£��������ݻ���Ϊ1 L���ܱ������У��ֱ����÷�Ӧ��
���� | �� | �� |
��Ӧ��Ͷ���� | 1 mol CO (g)��2 mol H2(g) | 1 mol CH3OH(g) |
ƽ��ʱc(CH3OH) | c1 | c2 |
ƽ��ʱ�����仯 | �ų�54kJ | ����a kJ |
��c1_________ c2(�������������),a=____________��
�����ܱ������ݻ������ͬ�������߷ֱ��ʾͶ�ϱȲ�ͬʱ�ķ�Ӧ���̡�����Ӧ��n(CO)��ʼ =10 mol��Ͷ�ϱ�Ϊ0.5����
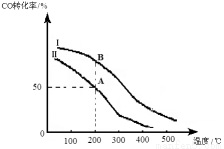
A���ƽ�ⳣ��KA= ��
B���ƽ�ⳣ��KB KA�� (�������������)
��Ϊ���COת���ʿɲ�ȡ�Ĵ�ʩ�� �����ٴ����������
��4�����NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��
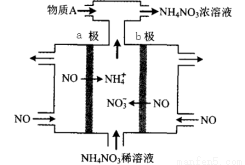
��a�缫����Ϊ_______��
b�缫��ӦʽΪ_________________��
 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶�3���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������漰��ѧ���֪ʶ��������ȷ����
A���ں�FeCl2���ʵ�FeCl3��Һ��ͨ����Cl2��ּ��ȣ���ȥ������Cl2�����ɵõ��ϴ�����FeCl3��Һ
B��10 g46%���Ҵ�ˮ��Һ��������ԭ����ĿΪ1.2NA
C��200 ml1mol/LFe2(SO4 )3��Һ�У�Fe3+��SO42-���������ܺ���NA
D�����õ���Ȼ�þ��Һ�ķ�����ȡ����þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���½���³ľ����������ڶ�������Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ�����������������������ء�����˵���в���ȷ����
A��ʳ�μȿ�����ζƷҲ����ʳƷ������
B����ˮ�м��뾻ˮ����������ʹ��ˮ����
C���Ӵ�ʯ�͡�ú̿�Ŀ����ٶȣ����ӻ�ʯȼ�ϵĹ�Ӧ�����ڡ����칤�̡��Ľ���
D������������ϴֲ������Ͻ���Ϊ���Ͻ�ǿ�ȴ������ᡢ����ʴ����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ֣���и����ڶ�������Ԥ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
(14��)CO��SO2����Ҫ�Ĵ�����Ⱦ���壬���û�ѧ��Ӧԭ����������Ⱦ����Ҫ������
I���״����Բ���Ͳ������ʯ��ȼ�ϣ�������Դ���š�����CO���Ժϳɼ״���
��2��һ�������£����ݻ�ΪVL���ܱ������г���� mol CO��2a mol H2�ϳɼ״�ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
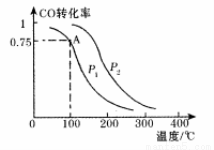
��P1�ߣ�P2(���������������=��)��������
�ڸü״��ϳɷ�Ӧ��A���ƽ�ⳣ��K= (��a��V��ʾ)
�۸÷�Ӧ�ﵽƽ��ʱ����Ӧ��ת���ʵĹ�ϵ��:CO H2(����� �������� ��=�� )
�����д�ʩ���ܹ�ͬʱ��������Ӧ���ʺ����COת���ʵ��� ��(��д��Ӧ��ĸ)
A��ʹ�ø�Ч����
B�����ͷ�Ӧ�¶�
C��������ϵѹǿ
D�����Ͻ�CH30H�ӷ�Ӧ������з������
E�����ӵ����ʵ�����CO��H2
��ijѧϰС����SO2Ϊԭ�ϣ����õ绯ѧ������ȡ���ᡣ
��3��ԭ��ط�:��С����Ƶ�ԭ���ԭ����ͼ��ʾ��д���õ�ظ����ĵ缫��Ӧʽ ��
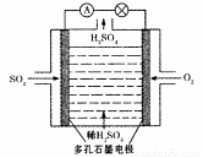
��4����ⷨ:��С����Na2SO3��Һ�������S02�õ�NaHSO3��Һ��Ȼ�������Һ�Ƶ������ᡣԭ������ͼ��ʾ��
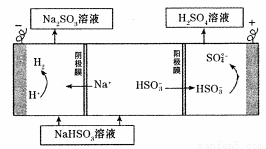
д����ʼ���ʱ�����ĵ缫��Ӧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ֣���и����ڶ�������Ԥ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ�Dz��ֶ�����Ԫ��ԭ������������������֮�ʵĹ�ϵͼ������˵������ȷ����

A��Ԫ�ض�Ӧ�����Ӱ뾶:Z��M��R��W
B�����⻯��ķе�:W��R��Y��X
C��M��N��R��W�ļ����Ӿ��ܴٽ�ˮ�ĵ���
D��Z��X��R��W������������Ӧ��ˮ���������N�ĵ��ʷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���������ظ���3��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ʵ�ķ���ʽ����ȷ����
A����0.01mol/L�Ĵ����pHΪ5��CH3COOH CH3COO- + H+
CH3COO- + H+
B����ⱥ��ʳ��ˮ���������壺2Cl- + 2H2O Cl2�� +2OH- + H2��
Cl2�� +2OH- + H2��
C��������������ȼ�գ�������ɫ���壺4Fe +3O2 2Fe2O3
2Fe2O3
D���������̼������Һ��������ɫ������CaSO4(S)+CO32- CaCO3(S)+SO42-
CaCO3(S)+SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱������ͷ��������3���ۺ���ϰ���ۻ�ѧ�Ծ��������棩 ���ͣ������
��16�֣��ϳ��л�������֬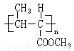 �߾���H�ĺϳ�·�����£�
�߾���H�ĺϳ�·�����£�

��֪��
RCOOR��+ R��OH  RCOOR�� + R��OH ��R��R�䡢R�����������
RCOOR�� + R��OH ��R��R�䡢R�����������
CH2=CH��CH=CH2��CH2=CH2 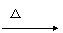

�Իش�
��1��E�й����ŵ������� ��
��2��C��D�ķ�Ӧ������ ��D��E��Ӧ�ġ�һ���������� ��
��3������˵����ȷ����(ѡ����ĸ) ��
A���ҿ�ʹBr2��CCl4��Һ��ɫ
B��G���Ҷ�����Ϊͬϵ��
C��D�ĺ˴Ź���������4��壬�ҷ����֮��Ϊ3:1:1:1
D�������л�������֬�߾���H��Ϊ�Ӿ۷�Ӧ
��4��B��C�Ļ�ѧ����ʽ�� ��
��5���ҵ�ͬ���칹���к����������� �֣�д�������ܷ���������Ӧ��һ��ͬ���칹��Ľṹ��ʽ ��
��6�����ɸ߾���H�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���з�ɽ������һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ͨ����ˮ��pH=8.1�����ȶ���ˮpH�������õ�������
A��Na+ B��HCO3- C��CO32- D��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��һ4���¿����ƻ�ѧ�Ծ��������棩 ���ͣ������
(9��)��Ҫ����գ��ش��������⡣
��1�����������У�ԭ�Ӱ뾶��С��Ԫ���ǣ�ϡ������Ԫ�س��⣩_____________����A���У��ǽ�������ǿ��Ԫ����_____________(��дԪ�ط���)��
��2��﨡��ȡ�������Ԫ���У��ʺ����뵼����ϵ��� ����Ԫ�����ƣ���
��3��XԪ�ص�ԭ�Ӻ�����2�����Ӳ㣬����L����5�����ӣ���Ԫ�������ڱ��е�λ��Ϊ ������̬�⻯��Ļ�ѧʽ �����������Ļ�ѧʽΪ ����Ԫ������������Ӧˮ���������⻯�ﷴӦ����Ļ�ѧʽΪ ��
��4����������A1N���������¡�������������Ժõ��������ʣ���ҵ����������������̼��һ�������·�Ӧ�Ƶ�AlN��CO���뽫���еĻ�ѧ��Ӧ����ʽ��ƽ��
Al2O3 + N2 + C �� AlN + CO
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com