
【题目】已知下列热化学方程式:
①H2O(l)=H2(g)+ ![]() O2(g) △H=+285.8 kJ/mol
O2(g) △H=+285.8 kJ/mol
②H2(g)+ ![]() O2(g)=H2O(g) △H=-241.8 kJ/mol
O2(g)=H2O(g) △H=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol
④C(s)+ ![]() O2(g)=CO(g) △H=-110.5 kJ/mol
O2(g)=CO(g) △H=-110.5 kJ/mol
⑤C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是____________________ 。
(2)C的燃烧热为____________________。
(3)燃烧10g H2生成液态水,放出的热量为______________。
(4)写出表示CO燃烧热的热化学方程式:__________________;写出制水煤气的热化学方程式:______________________。
【答案】 ① 393.5 kJ/mol 1429 kJ CO(g)+ ![]() O2(g) =CO2(g) △H=283.0 kJ/mol C(s)+H2O(g=CO(g)+H2(g) △H=+131.3 kJ/mol
O2(g) =CO2(g) △H=283.0 kJ/mol C(s)+H2O(g=CO(g)+H2(g) △H=+131.3 kJ/mol
【解析】试题分析:(1)吸热反应△H>0,因此①是吸热反应;(2)燃烧热:25℃时,1mol可燃物完全燃烧生成稳定氧化物所放出的热量,如C转化成CO2,H转化成液态水,因此⑤表示碳燃烧热的热化学反应方程式,即燃烧热:△H="-393.5" kJ/mol ;(3)②+①得出:H2O(l)=H2O(g) △H=+44kJ·mol-1⑥,②-⑥推出:H2(g)+1/2O2(g)=H2O(l) △H=-241.8-44kJ·mol-1=-285.8 kJ·mol-1,因此消耗10g氢气放出的热量为1429kJ;(4)⑤-④推出:CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ·mol-1;④-②得出:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ·mol-1。


科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )

A. AOa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O
B. ab段与cd段所发生的反应相同
C. de段沉淀减少是由于BaCO3固体消失的
D. bc段反应的离子方程式是2AlO2﹣+3H2O+CO2═2Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液中加入溴水后,溴被还原,由此推断该溶液中( )
A.不含NO3-,含Fe3+B.含有NO3-、I-、Cl-
C.含I-,但不能确定是否含Cl-D.含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象的解释不正确的是
选项 | 实验现象 | 解释 |
A | C12使鲜艳的红色花瓣褪色 | Cl2具有强还原性 |
B | NH3与HCl气体接触时有白烟产生 | NH3与HCl反应生成固体小颗粒 |
C | 新切开的Na表面在空气中很快变暗 | Na容易与空气中的氧气等反应 |
D | 氯化铝溶液中滴入过量的氢氧化钠溶液,白色沉淀溶解 | 氢氧化铝具有两性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答问题:
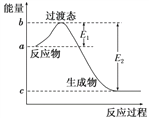
(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。
(2)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
(3)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为____________________________________________________________________。
(4)在微生物作用的条件下,NH经过两步反应被氧化成NO。这两步的能量变化如图:
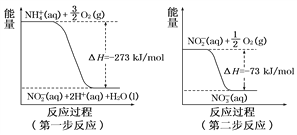
第二步反应是__________反应(填“放热”或“吸热”)。1 mol NH(aq)全部氧化成NO(aq)的热化学方程式是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com