
| A. | Ds原子在周期表中位于第7周期第ⅦB族 | |
| B. | Ds是过渡元素 | |
| C. | Ds原子的核外电子数为110 | |
| D. | Ds为金属元素 |
分析 根据原子序数=质子数=核外电子数可知,Ds的核外电子总数为100,根据118号元素可知该位于元素周期表中的第七周期第ⅤⅢ族,为金属元素,据此进行判断.
解答 解:A.原子序数为118应为第7周期0族元素,原子序数为110的元素位于第10个纵行,所以Ds位于元素周期表中的第七周期第ⅤⅢ族,故A错误;
B.Ds为ⅤⅢ族元素,属于过渡元素,故B正确;
C.原子序数=质子数=核外电子数=110,故C正确;
D.Ds处于第七周期第ⅤⅢ族,为过渡元素,属于金属元素,故D正确;
故选A.
点评 本题考查位置、结构与性质关系的应用,为高频考点,把握周期表结构及利用原子序数推断元素的位置为解答的关键,侧重基础知识的考查,注意掌握原子结构与元素周期表结构、元素周期律内容的关系.


科目:高中化学 来源: 题型:选择题
| A. | 偏大 | B. | 偏小 | C. | 无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
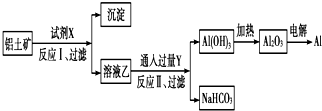
| A. | 试剂X为NaOH溶液 | |
| B. | 反应Ⅱ中生成Al(OH)3的反应为:CO2+[Al(OH)4]-═Al(OH)3↓+HCO3- | |
| C. | 结合质子(H+)的能力由强到弱的顺序是OH->[Al(OH)4]->CO32- | |
| D. | 工业上还可采用热还原法冶炼Al |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
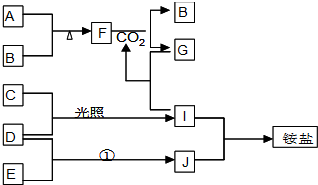
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
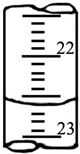 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:| 滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
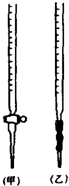 溶液中的离子反应
溶液中的离子反应查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 1 | 实验步骤 | 实验现象 |
| ⅰ.取2mL 1mol•L-1 KI溶液,滴加0.1mol•L-1 FeCl3溶液3滴(1滴约为0.05mL,下同). | ⅰ.溶液呈棕黄色. | |
| ⅱ.向其中滴加2滴0.1mol•L-1 KSCN溶液. | ⅱ.溶液不显红色. |
| 实验 2 | 实验步骤 | 实验现象 |
| ⅰ.取2mL 0.1mol•L-1 KI溶液,滴加0.1mol•L-1 FeCl3溶液3滴. | ⅰ.溶液呈棕黄色. | |
| ⅱ.向其中滴加2滴0.1mol•L-1 KSCN溶液. | ⅱ.溶液显红色. | |
| ⅲ.继续加入2mL CCl4,充分振荡、静置. | ⅲ.液体分层,上层红色消失,变为棕黄色,下层呈紫红色. |
| 实验3 | 实验步骤 | 实验现象 |
| ⅰ.取1mL实验2中棕黄色的上层清液,再加入2mL CCl4,振荡、静置. | ⅰ.液体分层,上层呈黄色,下层呈紫红色. | |
| ⅱ.取1mL饱和碘水,加入2mL CCl4,振荡、静置. | ⅱ.液体分层,上层为无色,下层呈紫红色. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
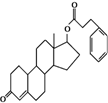
| A. | 含有四种官能团 | B. | 分子中所有碳原子不可能共平面 | ||
| C. | 是一种芳香族化合物 | D. | 含有一个酯基 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com