
| A. | 单质分子中一定不存在共价键 | |
| B. | 气态物质中一定有共价键 | |
| C. | 在共价化合物中一定有共价键 | |
| D. | 由非金属元素组成的化合物中,一定不含离子键 |
分析 A.双原子单质分子中存在共价键;
B.稀有气体的单质中不存在化学键;
C.只含有共价键的化合物属于共价化合物;
D.铵盐为离子化合物.
解答 解:A.双原子单质分子中存在共价键,如氢气中存在H-H共价键,故A错误;
B.因稀有气体的单质为单原子构成的分子,则不存在化学键,即单质分子中不一定存在共价键,故B错误;
C.只含有共价键的化合物属于共价化合物,所以在共价化合物中一定有共价键,故C正确;
D.铵盐为离子化合物,全部为非金属元素组成,则由非金属元素组成的化合物不一定是共价化合物,故D错误;
故选C.
点评 本题考查化学键,熟悉常见物质中的化学键及物质的性质是解答的关键,并学会利用举例的方法来解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
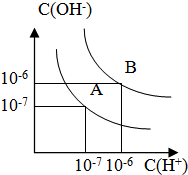 已知水在25℃和100℃时,其电离平衡曲线如图所示:
已知水在25℃和100℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY | B. | XY2 | C. | XY4 | D. | X2Y3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 其他条件不变,向平衡体系中再充入0.32mol A,再达平衡时,B的转化率增大 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v (逆)>v (正) | |
| C. | 其他条件不变,起始时向容器中充入各0.64mol A和B,平衡时n(C)<0.48mol | |
| D. | 反应前2 min的平均速率v(C)=0.004 mol•(L•min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl=NH4++Cl- | B. | NaHSO4=Na++HSO42- | ||
| C. | H2CO3=2H++CO32- | D. | CH3COOH→CH3++COOH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com