
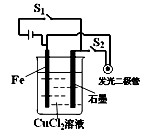
| A.断开开关S1,按下开关S2,化学能转化为电能,电能转化为光能等 |
| B.断开开关S1,按下开关S2,此时构成的装置属于电解池 |
| C.断开开关S2,按下开关S1,此时构成的装置属于原电池 |
| D.断开开关S2,按下开关S1,化学能转化为电能 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 C
C 。
。| 实验次数 | 稀橙汁体积(mL) | 滴定用标准碘(水)溶液(mL) |
| 1 | 25.00 | 23.10 |
| 2 | 25.00 | 23.00 |
| 3 | 25.00 | 22.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+
溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+| 滴定次数 | 待测草酸溶液体积(mL) | 0.1000 mol/LKMnO4标准溶液体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 10.02 |
| 第二次 | 25.00 | 0.22 | 11.32 |
| 第三次 | 25.00 | 1.56 | 11.54 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
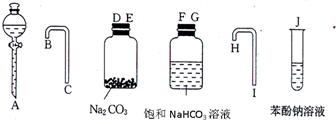
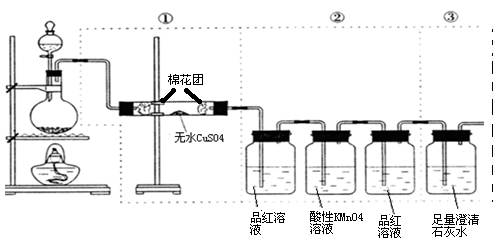
 园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装
园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装 通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题: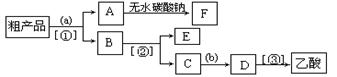
 。
。 分液,分离方法②是蒸馏,分离方法③是分液
分液,分离方法②是蒸馏,分离方法③是分液 ,乙酸和乙醇的酯化反应是分两步反应进行的,其反应的过程如下:
,乙酸和乙醇的酯化反应是分两步反应进行的,其反应的过程如下: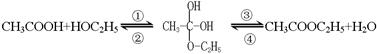
 基。为了探究酯化反应中的脱水方式,一般采取同位素示踪法,你认为用18O同位素进行标记时,下列标记正确的是 。
基。为了探究酯化反应中的脱水方式,一般采取同位素示踪法,你认为用18O同位素进行标记时,下列标记正确的是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| | A | B | C | D |
| 纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
| 小烧坏中的溶液 | 浓盐酸 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
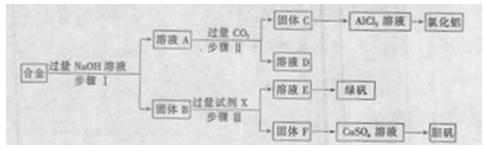
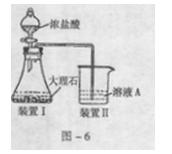
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
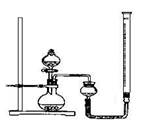
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 相关实验 | 预期目的 |
| A | 把等质量的两份同种大理石块中的一份研成粉末,在同温度下分别与等体积同浓度的盐酸反应,观察放出气体快慢。 | 验证接触面积对化学反应速率的影响。 |
| B | 把装有颜色相同的NO2与N2O4混合气体的小试管(密封)分别浸入热水和冷水中,观察试管中气体颜色变化。 | 验证温度对化学平衡的影响。 |
| C | 直接将表面积相同的铝条和镁条投入同温度滴有酚酞的热水中,观察产生气泡的速率及溶液的颜色变化。 | 比较同周期金属元素的金属性强弱。 |
| D | 将足量氯水分别滴入盛有溴化钠溶液和氯化钠溶液的试管中,观察溶液颜色变化。 | 验证溴元素和碘元素的非金属性强弱。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com