
(10分)A、B、C、 D、 E五种溶液分别是NaOH、NH3·H2O、CH3COOH 、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1 L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为: y<x;
②浓度均为0.1mol·L-1A和E溶液,pH:A<E;
③浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是 溶液。
(2)用水稀释0.1 mol·L-1B时,溶液中随着水量的增加而减小的是 (填写序号)
① ; ②
; ② ;
;
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(3)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是________(填写序号)
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率 E>A
⑤A溶液里有锌粉剩余 ⑥E溶液里有锌粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的_________曲线(填写序号)。

(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为 。
(1)NaOH(2)②(3) ③④⑤(4) ④(5) c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
【解析】
试题分析:(1)中和酸性物质A只有NaOH、NH3?H2O,物质的量的A与等物质的量浓度B和D混合呈中性,D的用量少,说明D碱性比B的碱性强,所以D是NaOH,根据浓度均为0.1mol?L-1C与D溶液等体积混合,溶液呈酸性,则C为NH4HSO4;故答案为:NaOH;(2)A、B溶液为氨水溶液,由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,则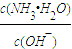 =
=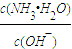 减小,故①错误;由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,c(NH3?H2O)、c(OH-)都减小,c(H+)减小,则
减小,故①错误;由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,c(NH3?H2O)、c(OH-)都减小,c(H+)减小,则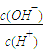 减小,故②正确;因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,故③错误;由NH3?H2O?OH-+NH4+可知,加水促进电离,OH-的物质的量增大,故④错误;故答案为:AB;(3)①根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,产生的氢气一样多,反应所需要的时间HCl>CH3COOH,故①错误;②根据酸能与锌反应得到氢气,开始溶液中c(H+)相等,反应时的速率HCl=CH3COOH,故②错误;③根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故③正确;④根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,故④正确;⑤根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑤正确;⑥根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑥错误;故答案为:③④⑤;(4)等体积、等物质的量浓度NH3?H2O和与NH4HSO4混合后溶液发生反应:NH3?H2O+NH4HSO4=(NH4)2SO4+H2O,NH4)2SO4要发生水【解析】
减小,故②正确;因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,故③错误;由NH3?H2O?OH-+NH4+可知,加水促进电离,OH-的物质的量增大,故④错误;故答案为:AB;(3)①根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,产生的氢气一样多,反应所需要的时间HCl>CH3COOH,故①错误;②根据酸能与锌反应得到氢气,开始溶液中c(H+)相等,反应时的速率HCl=CH3COOH,故②错误;③根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故③正确;④根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,故④正确;⑤根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑤正确;⑥根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑥错误;故答案为:③④⑤;(4)等体积、等物质的量浓度NH3?H2O和与NH4HSO4混合后溶液发生反应:NH3?H2O+NH4HSO4=(NH4)2SO4+H2O,NH4)2SO4要发生水【解析】
NH4++H2O?NH3?H2O+H+,溶液呈酸性,加热水解平衡正向移动,c(H+)增大,pH减小,故答案为:④;(5)NH4HSO4中滴入NaOH溶液,NaOH首先与NH4HSO4电离出的H+作用,因为H+结合OH-的能力比NH4+结合OH-的能量强(原因是产物H2O比NH3?H2O更难电离).当加入等摩尔的NaOH时,正好将H+中和,此时c(Na+)=c(SO42-),但此时溶液中还有NH4+,NH4+水解使溶液呈酸性,因此要使溶液呈中性,则还需继续滴入NaOH,当然到中性时c(OH-)=c(H+),c(Na+)>c(SO42- )>c(NH4+),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
考点:电解质溶液、离子浓度比较


科目:高中化学 来源:2014-2015浙江省高二1月月考化学试卷(解析版) 题型:实验题
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4++6HCHO=3H++6H2O+(CH2)6N4H+(滴定时,1 mol(CH2)6N4H+与 l mol H+相当),然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g。
步骤II:将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数 (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积 (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察 。
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④判断滴定终点的现象是 。
⑤如图是某次滴定时的滴定管中的液面,其读数为 mL。

(2)滴定结果如下表所示:

若NaOH标准溶液的浓度为0.1050mol·L-1则该样品中氮的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
反应FeO(s)+C(s)=Fe(s)+CO(g);△H>0,ΔS>0,下列说法正确的是
A.低温下自发进行,高温下非自发进行 B.高温下自发进行,低温下非自发进行
C.任何温度下均为非自发进行 D.任何温度下均为自发进行
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省平度市高二上学期期中考试化学试卷(解析版) 题型:选择题
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达平衡时,X的转化率为50%
B.反应可表示为:X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.当混合气体的平均相对分子质量不变时,该反应达到了化学平衡状态
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省平度市高二上学期期中考试化学试卷(解析版) 题型:选择题
在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
A.x=2
B.2 min内A的反应速率为0.6 mol·L-1·min-1
C.B的转化率为40%
D.若混合气体的密度不变,则表明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH 溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)根据图示判断,下列说法正确的是

A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C.欲使NaHA溶液呈中性,可以向其中加入酸或碱
D.向NaHA溶液加入水的过程中,pH可能增大也可能减少
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
下表是某铬酸(H2CrO4)溶液中离子浓度(mol·L-1)与pH的关系,下列说法不正确的是
pH | c(CrO42-) | c(HCrO4-) | c(Cr2O72-) | c(H2CrO4) |
4 | 0.0003 | 0.1040 | 0.4480 | 0 |
6 | 0.0319 | 0.0999 | 0.4370 | 0 |
7 | 0.2745 | 0.0860 | 0.3195 | 0 |
9 | 0.9960 | 0.0031 | 0.0004 | 0 |
A.铬酸的第一步电离是完全电离
B.铬酸的第二步电离是部分电离,且存在两种电离方式
C.pH越大,电离出的CrO42-浓度越大
D.当电离达到平衡时,2v逆(Cr2O72-)= v正(HCrO4-)
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高二1月月考化学试卷(解析版) 题型:选择题
下列离子组能大量共存的是
A.使甲基橙呈红色的溶液中K+ 、Na+ 、NO3-、S2O32-
B.NH4+、Fe3+、CO32-、CH3COO-
C.使酚酞变红色的溶液中: Na+、 Cl-、K+、AlO2-
D.无色透明溶液中:SO32-、Cl-、K+、Cr2O72-
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二12月月考化学(选修)试卷(解析版) 题型:选择题
CPAE是蜂胶的主要活性成分,也可由咖啡酸合成

下列说法不正确的是
A.该反应是取代反应
B.可用金属Na检测上述反应是否残留苯乙醇
C.咖啡酸不能使酸性KMnO4溶液褪色
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com