
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________ ______________________________________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子反应方程式: 。
若要确认其中有Fe2+,应选用 (选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应的化学方程式为: 。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为 。
(1)铁表面被钝化
(2)①Fe+2H+=Fe2++H2↑ Fe+ 2Fe3+=3Fe2+ d
②SO2+Br2+2H2O = 2HBr+H2SO4 66.7%
解析试题分析:(1)铁在冷的浓硫酸中钝化,表面生成一层致密的氧化物保护膜,铁与CuSO4溶液被隔离。
(2)①随着反应的进行,硫酸的浓度逐渐减小,变为稀硫酸后,铁与稀硫酸反应生成硫酸亚铁,Fe过量,能与Fe3+反应生成Fe2+,离子方程式为:Fe+2H+=Fe2++H2↑ Fe+ 2Fe3+=3Fe2+;因为溶液含有Fe3+,所以不能用a、b、c项检验Fe2+,可利用Fe2+的还原性,用酸性KMnO4溶液检验Fe2+,故d项正确。
②Br2具有氧化性,SO2具有还原性,发生氧化还原反应,化学方程式为:SO2+Br2+2H2O = 2HBr+H2SO4;2.33g为BaSO4的质量,根据S元素守恒可知:SO2~ BaSO4,n(SO2)=n(BaSO4)=2.33g÷233g/mol=0.01mol,所以SO2的体积分数为:0.01mol×22.4L/mol÷0.336L×100%= 66.7% 。
考点:本题考查物质的性质、方程式的书写、离子的检验,体积分数的计算。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
某厂的酸性工业废水中含有一定量的Na+、Al3+、 Fe3+、Cu2+、Cl-。该厂利用如图所示的工艺流程图,利用常见的气体氧化物、酸、碱和工业生产中的废铁屑,从废水中生产出了氯化铁、氧化铝、NaCl晶体和金属铜,产生了很好的社会经济效益。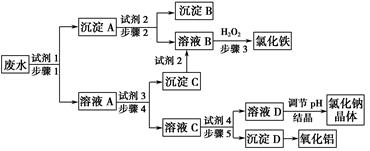
请填写下列空白:
(1)图中试剂1是________,试剂2是________。
(2)步骤1和步骤2所用到的玻璃仪器是________。
(3)步骤1反应的离子方程式为_______________________________________。
(4)步骤3反应的离子方程式为_______________________________________。
(5)从节约药品和环保方面考虑,步骤5所发生反应的离子方程式应为__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某不锈钢(主要成分为Fe)样品中含有铝、铜等(其它成分忽略),为了测定该合金中铁的含量,有人设计如下工艺流程:
(1)滤液C中溶质含有_ _(写化学式);
(2)如何验证滤液A中含Fe2+,而不含Fe3+____ _____。
(3)对所得Fe2O3固体称量得质量为b g,计算该样品中铁元素质量分数的表达式为(用含a、b的式子表示)___ __。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下: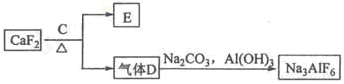
回答下列问题:
(1)写出反应1的离子方程式 , ,
(2)滤液Ⅰ中加入CaO生成的沉淀是 (填化学式),反应2(气体A足量)的离子方程式为 ;
(3)电解制铝的化学方程式是 ;
(4)C为浓硫酸,E为硫酸钙,写出由D制备冰晶石(有A生成)的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用含有Al2O3及少量Fe2O3和SiO2的铝土矿制备净水剂——液体聚合硫酸铝铁,工艺流程如下(部分操作和条件略):
I.向铝土矿中加入过量H2SO4后,加热、搅拌、过滤。
II.向滤液中加入一定量的FeSO4·7H2O和双氧水。
III.向溶液中加入Ca(OH)2固体,调节溶液的pH约为1,过滤。
IV.加入稳定剂,加热,得到产品。
(1)Fe2O3与H2SO4反应的离子方程式是___________。
(2)步骤I中过滤得到的滤渣成分是________(填化学式)。
(3)步骤I 中H2SO4的浓度与反应温度会影响铁与铝的浸出率。根据下图分析,步骤I 中H2SO4浓度的适宜范围是__________,反应的适宜温度是_________。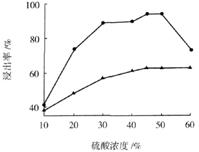

(4)步骤II中增大n(Fe3+)的离子方程式是_________。
(5)步骤III得到碱式硫酸铝铁[AlFe(OH)n(SO4)m]的溶液,则步骤II中应增大n(Fe3+)到
n(Al3+)﹕n(Fe3+)= 。
(6)研究表明,液体聚合硫酸铝铁的纯度越高,净水效果越好。已知:
一些物质在20℃时的溶解度
| 物质 | Ca(OH)2 | CaSO4 | Na2SO4 |
| 溶解度/g | 0.153 | 0.258 | 19.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某兴趣小组用废铁泥(主要成分为Fe2O3、FeO和少量Fe)制备磁性Fe3O4纳米材料的流程示意图如下: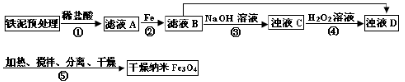
|
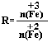 ,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。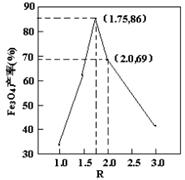
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO32-、Cl-、NO3-等离子中的若干种。现做如下实验:
一、取少量该溶液,滴入用硝酸酸化的AgNO 3溶液,有白色沉淀生成。
二、另取部分溶液,加入氢氧化钠,有白色沉淀产生,加入氢氧化钠的量与生成白色沉淀的量可用下图表示。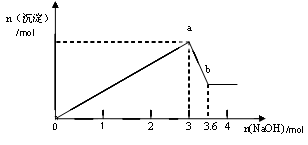
试推断:
(1)该溶液中一定存在__________ ____,一定不存在________________。
(2)由图可知白色沉淀共有__________种,分别是__________________(填化学式),其物质的量比为 。
(3) 写出图中a b变化过程的离子方程式 。
b变化过程的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁黄是一种重要的颜料,化学式为Fe2O3·xH2 O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含FeZ 0。及少量的CaO, Mg0等)和黄铁矿粉
(主要成分为FeS2)制备铁黄的流程如下: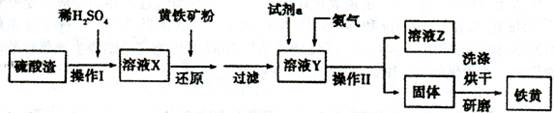
(1)操作I与操作II中都用到玻璃棒,玻璃棒在两种操作中的作用分别是_ 、
(2)试剂a最好选用_ (供选择使用的有:铝粉、空气、浓HNO3 );其作用是_ 。
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_ _(填序号)。
(4)查阅资料知,在不同温度下Fe2 O3被CO还原,产物可能为Fe3 O4 、FeO或Fe,固体质量与反应温度的关系如右图所示。根据图象推断670℃时Fe2 O3还原产物的化学式为M,并设计一个简单的实验,证明该还原产物的成分(依次填写每步操作中所加试剂的化学式、现象和结论)。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2 O2溶液、NaOH溶液、KSCN溶液。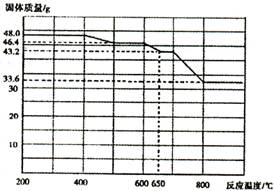
| 加入试剂 | 现象 | 结论 |
| | | 则还原产物为 |
| | | |
| | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有关物质间转化关系如下图,试回答: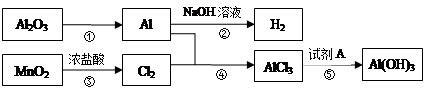
(1)转化①的反应条件为 .
(2)转化②的化学方程式为 .转化③的离子方程式为 .
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 (填名称).
(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为 mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com