
(1)画出装置图,并指出正极为__________,电极反应式为_______;负极为_______,电极反应式为________。
(2)若电池内溶液为100 mL 0.5 mol·L-1的FeCl3溶液;当溶液中FeCl3全部被还原成FeCl2时,溶液中ZnCl2的物质的量浓度是__________,导线上通过的电子是__________mol。
解析:自发发生的氧化反应的是Zn+2FeCl3====2FeCl2+ZnCl2,发生氧化反应的是Zn―2e-====Zn2+,发生还原反应的是2Fe3++2e-====2Fe2+,所以负极材料应为锌电极,正极材料应采用金属性比Zn弱的金属材料或非金属导电材料如石墨棒等,电解质溶液用FeCl3溶液。其装置图如图4-19所示。
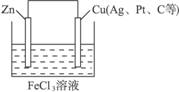
图4-19
负极为Zn,电极反应式:Zn―2e-====Zn2+;正极为Cu(或Ag、Pt、C等),电极反应式:2Fe3++2e-====2Fe2+。
(2)设n(Zn2+)=x,n(e-)=y,根据电池总反应可知
2Fe3++Zn====Zn2++2Fe2+转移电子的物质的量
2 mol 1 mol 1 mol 2 mol
0.05 mol x y
得x=0.025 mol,y=0.05 mol
c(ZnCl2)=0.025 mol/0.1 L=0.25 mol·L-1
导线上通过的电子的物质的量为0.05 mol。
答案:(1)Cu(或Ag、Pt、C等) 2Fe3++2e-====2Fe2+ Zn Zn-2e-====Zn2+
(2)0.25 mol·L-1 0.05


科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013届山东省青岛二中高三上学期9月阶段性检测化学试卷(带解析) 题型:填空题
(7分)二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下: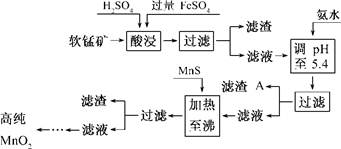
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | pH |
| Al(OH)3 | 5.2 |
| Fe(OH)3 | 3.2 |
| Fe(OH)2 | 9.7 |
| Mn(OH)2 | 10.4 |
| Cu(OH)2 | 6.7 |
| Zn(OH)2 | 8.0 |
| CuS | ≥-0.42 |
| ZnS | ≥2.5 |
| MnS | ≥7 |
| FeS | ≥7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省烟台市高三(上)期末化学试卷(解析版) 题型:解答题

| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com