
����Ŀ����Ȳ���ڴ��������¿ɷ���ż����Ӧ����ΪGlaser��Ӧ��
2R��C��C��H![]() R��C��C��C��C��R+H2
R��C��C��C��C��R+H2
�÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�
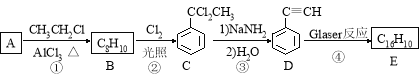
�ش��������⣺
��1��B�Ľṹ��ʽΪ ��D �Ļ�ѧ����Ϊ ��
��2���ٺ͢۵ķ�Ӧ���ͷֱ�Ϊ �� ��
��3��E�Ľṹ��ʽΪ ����1 mol E�ϳ�1��4-���������飬��������Ҫ��������_______mol��
��4��������(HC��C![]() C��CH)Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_______________________��
C��CH)Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_______________________��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1��д������һ�ֵĽṹ��ʽ_____________________��
��6��д����2-�����Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·�� ��
���𰸡���1��![]() ������Ȳ
������Ȳ
��2��ȡ����Ӧ����ȥ��Ӧ
��3��![]() 4
4
��4��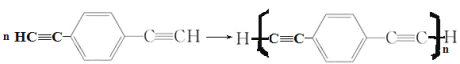 +(n-1)H2
+(n-1)H2
��5��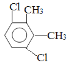 ��
��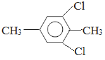 ��
��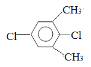 ��
��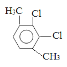 ��
��
��6��![]()
��������
�����������1��A�������鷢��ȡ����Ӧ����B�������B����ʽ��֪A�DZ���B�DZ����飬��B�Ľṹ��ʽΪ![]() ������D�Ľṹ��ʽ��֪D �Ļ�ѧ����Ϊ����Ȳ��
������D�Ľṹ��ʽ��֪D �Ļ�ѧ����Ϊ����Ȳ��
��2�����DZ�������ԭ�ӱ��һ�ȡ��������ȡ����Ӧ�����в���̼̼��������±��������ȥ��Ӧ��
��3��D������֪��Ϣ�ķ�Ӧ�����E�Ľṹ��ʽΪ![]() ��1��̼̼������Ҫ2���������ӳɣ�����1 mol E�ϳ�1��4-���������飬��������Ҫ��������4mol��
��1��̼̼������Ҫ2���������ӳɣ�����1 mol E�ϳ�1��4-���������飬��������Ҫ��������4mol��
��4��������֪��Ϣ��֪������![]() ����Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪ
����Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪ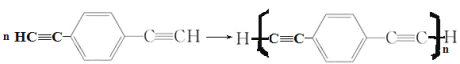 +(n-1)H2��
+(n-1)H2��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1���ṹ��ʽΪ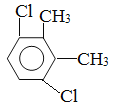 ��
��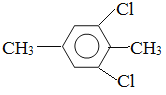 ��
��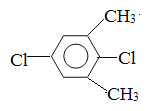 ��
��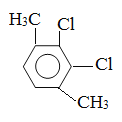 ��
��
��6��������֪��Ϣ�Լ��Ҵ������ʿ�֪��2-�����Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��Ϊ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ﮱ���Ϊ������ζ��������LiCoO2Ϊ�������ϵ�����ӵ���ѱ��㷺������Яʽ��Դ����ҵ�ϳ��Ԧ�﮻Կ�(��Ҫ�ɷ�ΪLiAlSi2O6��������FeO��MgO��CaO������)Ϊԭ������ȡ����ﮡ�����һ�ֹ����������£�
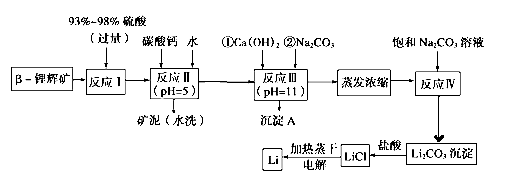
��֪��
�ٲ��ֽ����������↑ʼ��������ȫ����ʱ��pH��
�������� | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
��ʼ����pH | 2��7 | 3��7 | 9��6 |
��ȫ����pH | 3��7 | 4��7 | 11 |
��Li2CO3�ڲ�ͬ�¶��µ��ܽ�����±���
�¶�/�� | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3���ܽ��/g | 1��539 | 1��406 | 1��329 | 1��181 | 0��866 | 0��728 |
��ش��������⣺
��1������������ʽ��ʾLiAlSi2O6����ɣ�_______________________
��2����Ӧ�����̼��Ƶ�������____________________
��3��д����Ӧ�������ɳ���A�����ӷ���ʽ��____________________
��4��ϴ������Li2CO3����Ҫʹ�á���ˮ�����ǡ���ˮ��������____________________
��5������������ʹ����Na2CO3��Һ����һ��Ũ��С���ڶ���Ũ�ȴ��ԭ����____________________
��6���ù����У���������Ȼ�������ʱ�����������������л��������������ԭ����____________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ������Ǹ�ˮ�����װ����ͼ��ʾ�� �漰�Ļ�ѧ����ʽ���£�
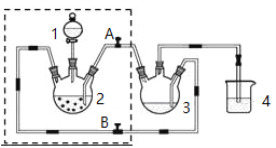
Zn��s��+2HCl��aq��= ZnCl2��aq��+H2��g����
2CrCl3��aq��+Zn��s��= 2CrCl2��aq��+ZnCl2��aq��
2Cr2+��aq��+4CH3COO����aq��+2H2O��l��=[Cr��CH3COO��2]22H2O ��s��
�����Ǹ�ˮ���[Cr��CH3COO��2��]22H2O�����ɫ���壩��һ���������ռ���ͨ���Զ�������Ӵ��ڣ���������ˮ���ѣ����ڴ������������ᡣ
��ش��������⣺
��1����������װ�������Եķ�����_____________________________________��
��2����ʵ��������������Һ��ˮ����У���ԭ����_________________________________��װ��4��������_________________________��
��3�������ɵ�CrCl2��Һ��CH3COONa��Һ���ʱ�IJ�����_________����A��__________����B ������رա�����
��4����ʵ����п�����������ԭ����__________________________________��
��5��Ϊϴ��[Cr��CH3COO��2��]22H2O��Ʒ�����з��������ʺϵ���________________��
A����������ϴ��������ˮϴ
B��������ˮϴ�������Ҵ�ϴ
C��������ˮϴ����������ϴ
D�������Ҵ�ϴ�ӣ���������ϴ
��6����Ԫ���ںܶ�������Ӧ�á��Ȼ�����(CrO2Cl2)���л��ϳ��п������������Ȼ��������������л��ﷴӦ��д����Ԫ�صĻ�̬ԭ����Χ�����Ų�ʽ��_________________�����ͬ���ڵ�����Ԫ�صĻ�̬ԭ�����������������ԭ����ͬ��Ԫ����_______________�������ƣ���CrO2Cl2������Ϊ���ɫҺ�壬����CCl4��CS2�Ȼ��ܣ��ݴ˿��ж�CrO2Cl2��________������ԡ��Ǽ��ԡ������ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г�ȥ���ʵIJ����д������
A����ȥʯӢ��������̼��ƣ���ϡ�����ܽ�����
B��FeCl2��Һ�л��е�FeCl3��������������۳�ַ�Ӧ�����
C����ȥ�������������е��������������ķ���
D���������������Ȼ������壺���������ͨ��ʢNaOH��Һ��ϴ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڰ���٤������NA������˵����ȷ���ǣ� ��
A. ���³�ѹ�£�1mol�����к��й��ۼ�Ϊ4NA
B. ��״���£�22.4L�״���ȫȼ�ղ���NA��CO2����
C. ���³�ѹ�£�46g NO2��N2O4������У�������ΪNA
D. 1L1mol/L Na2CO3��Һ�У������Ӹ�������NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2S2O3�׳ƴ��մ���������Ҫ�Ļ���ԭ�ϡ���Na2SO3�������ˮ��Һ�м��ȷ�Ӧ�������Ƶ�Na2S2O3����֪10����70��ʱ��Na2S2O3��100gˮ�е��ܽ�ȷֱ�Ϊ60.0g��212g�������£�����Һ�������ľ�����Na2S2O3��5H2O��
��ʵ��������ȡNa2S2O3��5H2O���壨Na2S2O3��5H2O�ķ�����Ϊ248���������£�
�ٳ�ȡ12.6g Na2SO3���ձ��У�����80.0mLˮ��
����ȡ4.0g��ۣ��������Ҵ���ʪ�ӵ�������Һ�С�
�ۣ���ͼ��ʾ������װ����ȥ����ˮԡ���ȣ��У���ӦԼ1Сʱ����ˡ�
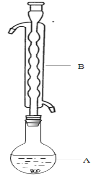
����Һ�ھ��� �� ������Na2S2O3��5H2O���塣
�ݽ��м�ѹ���˲����
��1������B��������________����������___________�������������Ҵ���ʪ��Ŀ���� ��
��2�������Ӧ��ȡ�IJ����� �� ��
��3����Һ�г�Na2S2O3�Ϳ���δ��Ӧ��ȫ��Na2SO3�⣬����ܴ��ڵ��������� �������Һ�и����ʵĺ������ܵͣ�����ķ����ǣ� ��
��4��Ϊ�˲��Ʒ�Ĵ��ȣ���ȡ7.40g ��Ʒ�����Ƴ�250mL��Һ������Һ����ȡ25.00mL����ƿ�У��μ�������Һ��ָʾ��������Ũ��Ϊ0.0500mol/L �ĵ�ˮ���� �����ʽ����ʽ�����ζ������ζ���2S2O32�� + I2 �� S4O62�� + 2I�������ζ�������£�
�ζ����� | �ζ�ǰ������mL�� | �ζ��ζ��������mL�� |
��һ�� | 0.30 | 31.12 |
�ڶ��� | 0.36 | 31.56 |
������ | 1.10 | 31.88 |
�����ò�Ʒ�Ĵ���Ϊ ������ΪӰ�촿�ȵ���Ҫԭ���ǣ������Dz��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ��ѡ��5 �л���ѧ������
ij���᳦��ҩ����Ч�ɷֵĺϳ�·������(���ַ�Ӧ��ȥ�Լ�������)��
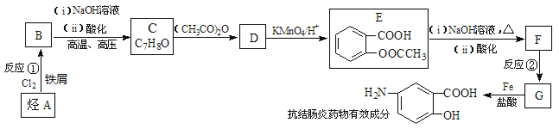
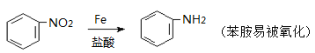
��֪��
��ش��������⣺
��1�����᳦��ҩ����Ч�ɷֵķ���ʽ���� ����A������Ϊ�� ����Ӧ�ڵķ�Ӧ�������� ��
��2�������жԸÿ��᳦��ҩ����Ч�ɷֿ��ܾ��е������Ʋ���ȷ������ ��
A��ˮ���Աȱ��Ӻ�
B���ܷ�����ȥ��ӦҲ�ܷ����ۺϷ�Ӧ
C��1mol������������4mol H2������Ӧ
D���������������
�� E������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ���� ��
��3���������������Ŀ��᳦��ҩ����Ч�ɷֵ�ͬ���칹����______����
A����FeCl3��Һ����ɫ��Ӧ
B�������м��뱽��ֱ������
C�������Ϲ�������ȡ����
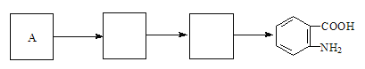
��4����֪���������������ʱ������һ��ȡ��������ȡ����������ڶ�λ�����������������Ȼ�ʱ��ȡ���ڼ�λ,�ݴ˰��Ⱥ�˳��д����AΪԭ�Ϻϳ��ڰ���������(![]() )�ϳ�·���������м����Ľṹ��ʽ(���ַ�Ӧ��������ȥ)
)�ϳ�·���������м����Ľṹ��ʽ(���ַ�Ӧ��������ȥ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ij�����һЩԪ�ض���������뵼����ϣ������ǣ� ��
A. ϡ������Ԫ��
B. ���·�����Ľ���Ԫ��
C. ���Ϸ�����ķǽ���Ԫ��
D. ����Ԫ�غͷǽ���Ԫ�طֽ��߸�����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������±�ص�ԭ�Ӱ뾶���������еݱ������ȷ���ǣ� ��
A. ���ʵ��۵����� B. ±�����ӻ�ԭ������ǿ
C. ��̬�⻯���ȶ�������ǿ D. ��������������ǿ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com