
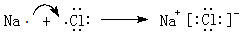 .
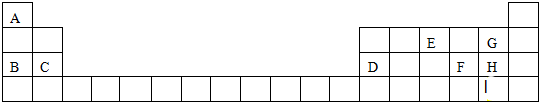
.分析 由元素在周期表中位置,可知A为氢,B为Na,C为Mg,D为Al,E为氮,F为硫,G为氟,H为Cl,I为Br.
(1)第三横行为第三周期,第16列为VIA族;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大;非金属性越强,氢化物越稳定;
(3)氧化铝属于两性氧化物;金属性越强,最高价氧化物对应水化物的碱性越强;
(4)B、H形成化合物NaCl,由钠离子与氯离子构成;
(5)利用单质相互置换反应可以等说明单质氧化性强弱.
解答 解:由元素在周期表中位置,可知A为氢,B为Na,C为Mg,D为Al,E为氮,F为硫,G为氟,H为Cl,I为Br.
(1)第三横行为第三周期,第16列为VIA族,故F处于第三周期VIA族,
故答案为:三、VIA;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故上述元素中Na的原子半径最大;E、F、G、H中氟元素非金属性最强,故HF最稳定,
故答案为:Na;HF;
(3)Al2O3属于两性氧化物;Na的金属性最强,故NaOH的碱性最强,
故答案为:Al2O3;NaOH;
(4)B、H形成化合物NaCl,由钠离子与氯离子构成,用电子式表示形成过程为: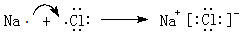 ,
,
故答案为: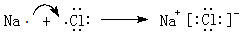 ;
;
(5)比较氯气、溴单质氧化性的强弱的实验方案为:在NaBr溶液中滴加Cl2水,若溶液加深(有红棕色形成),说明Cl2的氧化性比Br2强,
故答案为:在NaBr溶液中滴加Cl2水,若溶液加深(有红棕色形成),说明Cl2的氧化性比Br2强.
点评 本题考查元素周期表与元素周期表,旨在考查学生对基础知识的巩固,掌握用电子式表示物质或化学键形成,掌握金属性、非金属性强弱比较.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题

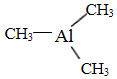 ,则其中铝原子的杂化方式为sp2.若氮化铝可由(CH3)3Al 和 NH3在一定条件下反应制得,反应的方程式为:(CH3)3Al+NH3$\frac{\underline{\;一定条件\;}}{\;}$AlN+3CH4 ,该反应与取代反应有机反应类型相似(填反应名称).
,则其中铝原子的杂化方式为sp2.若氮化铝可由(CH3)3Al 和 NH3在一定条件下反应制得,反应的方程式为:(CH3)3Al+NH3$\frac{\underline{\;一定条件\;}}{\;}$AlN+3CH4 ,该反应与取代反应有机反应类型相似(填反应名称).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
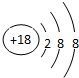 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加澄清的石灰水 | B. | 两者分别与同浓度的稀盐酸反应 | ||
| C. | 溶于水,比较其溶解性 | D. | 两者分别加入NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤是工业上获得苯、甲苯、二甲苯等芳香烃的重要来源 | |
| B. | 煤是由多种有机化合物组成的混合物,内含煤焦油等成分 | |
| C. | 煤除了含有C、H元素外,还含有少量的N、S、O等元素 | |
| D. | 煤等化石燃料的储量有限,节能和开发新能源是人类实现可持续发展的关键之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和水反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O | |
| C. | 碳酸氢钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 工业上电解饱和食盐水的反应:2Na++2Cl-$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将 SO2 通入水中 | B. | 将 HCl 通入水中 | C. | 烧碱溶于水 | D. | 硫酸氢钾溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com