
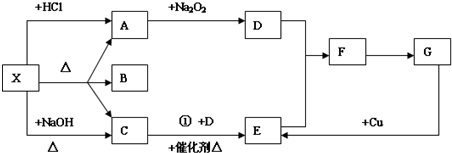
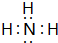
分析 常温下A、C是无色气体,A是能使澄清石灰水变浑浊的无色无味气体,则A为CO2,C能使湿润的红色石蕊试纸变蓝,则C为NH3,B是常见无色液体,则B为H2O,X即能与酸反应又能与碱反应,X加热生成A、B、C物质的量相等,X为NH4HCO3,A与过氧化钠反应生成D,氨气能与D连续反应生成F,则D为O2,氨气催化氧化生成E为NO,E与D反应生成F为NO2,F转化生成G,而G可与Cu反应生成NO,则G为HNO3,据此答题.
解答 解:常温下A、C是无色气体,A是能使澄清石灰水变浑浊的无色无味气体,则A为CO2,C能使湿润的红色石蕊试纸变蓝,则C为NH3,B是常见无色液体,则B为H2O,X即能与酸反应又能与碱反应,X加热生成A、B、C物质的量相等,X为NH4HCO3,A与过氧化钠反应生成D,氨气能与D连续反应生成F,则D为O2,氨气催化氧化生成E为NO,E与D反应生成F为NO2,F转化生成G,而G可与Cu反应生成NO,则G为HNO3.
(1)物质X是NH4HCO3,C是NH3,故答案为:NH4HCO3;NH3;
(2)A为CO2,结构式为:O=C=O,C为NH3,电子式为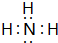 ,故答案为:O=C=O;
,故答案为:O=C=O;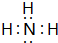 ;
;
(3)X加热分解的化学方程式:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,故答案为:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑;
(4)反应①的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(5)F→G的化学方程式:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
(6)G→E的离子方程式:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,故答案为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑.
点评 本题考查无机物推断,“常温下A、C为无色气体,C能使湿润的红色石蕊试纸变蓝,X能与盐酸、氢氧化钠反应”等是推断突破口,需要学生熟练掌握元素化合物性质,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
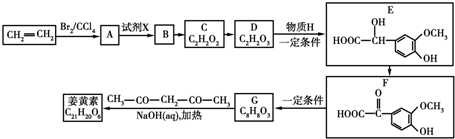


 .
.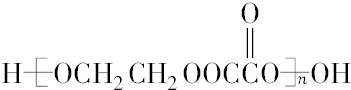 .
.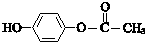 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
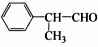 ,工业合成路线如下:
,工业合成路线如下: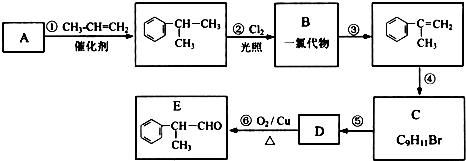
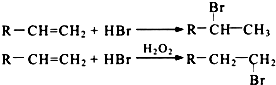 (R-代表烃基)
(R-代表烃基) 或
或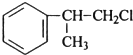 (任写一个),其官能团为氯原子.
(任写一个),其官能团为氯原子.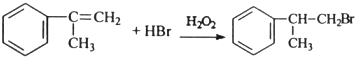 (必须有反应条件).
(必须有反应条件). .
.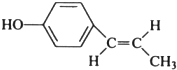 (只写反式结构).
(只写反式结构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 石油裂解主要目的是得到短链的不饱和烃 | |
| D. | 煤的气化与液化都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
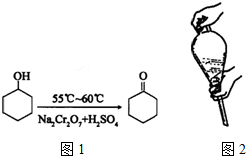
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3、20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44g14C1802所含有的中子数为28NA | |
| B. | 32gCH4中所含共价键数为8NA | |
| C. | 7.8gNa2O2固体中所含离子数为0.4NA | |
| D. | 17gOH-所含有的电子数为9NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com