
| | 实验操作 | 实验  目的 目的 |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠中含有醛基 |
| B | 向苯酚的饱和溶液中滴加稀溴水 | 看到三溴苯酚沉淀 |
| C | 向酒 精和醋酸的混合液中加入金属钠 精和醋酸的混合液中加入金属钠 | 确定酒精中混有醋酸 |
| D | 将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的溴离子 |
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:填空题
 mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程:
mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。完成以下实验探究过程: 作、预期现象和结论。
作、预期现象和结论。| 编号 | 实验操作 | 实验现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量  ____ 溶液并滴加到试管A中,充分反应 ____ 溶液并滴加到试管A中,充分反应 | 有固体剩余,并有气泡产生 | 合金中除铝外还含有Fe、Cu 元素 |
| ② | 往试管A的剩余固体中加过量 ________ ,充分反应后,静置,取上层清液于试管B中 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | |
| ③ | 往试管B中加入少量 _____,再滴加KSCN溶液 | _____ | |
| ④ | 往②剩余固体中加入稀硝酸;再滴加 ____________ 溶液. | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色;再加某溶液后有蓝色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑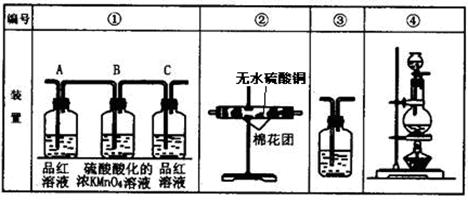
 接顺序(按产物气流从左到右的方向)是(填装置的编号):
接顺序(按产物气流从左到右的方向)是(填装置的编号): ④ →__________→__________→__________。
④ →__________→__________→__________。| A.BaCl2溶液 | B.Ba(OH)2溶液 |
| C.滴加H2O2的BaCl2溶液 | D.滴加H2O2的Ba(OH)2溶液 |
 增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
增重质量为bg。用a、b表示CO2和SO2的物质的量比 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验操作 | 实验现象 | 实验结论 |
| A | 向某溶液中加入稀盐酸,并将产生的气体通入澄清石灰水中 | 无色无味的气体使澄清石灰水变浑浊 | 原溶液中含有CO32? |
| B | 二氧化硫通入溴水中 | 溶液褪色 | 二氧化硫有漂白性 |
| C | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| D | 取少量某无色溶液,先滴加氯水,再加入少量四氯化碳,振荡、静置 | 溶液分层,下层呈橙红色 | 原无色溶液中一定有溴离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.检验C2H5Cl中的氯元素时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸后进行酸化,再加硝酸银溶液 |
| B.向溶液中加入盐酸,有无色气体逸出,此气体能使澄清石灰水变浑浊,则该溶液中含有CO32- |
| C.向0.1mol·L-1 FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性 |
| D.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1 AgNO3溶液,振荡,沉淀呈黄色,说明AgCl 的Ksp比AgI 的Ksp大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2通入酸性高锰酸钾溶液中,溶液褪色,说明SO2具有漂白性 |
| B.用蒸馏水将PH试纸先润湿,可用于检验氨气 |
| C.可用瓷坩埚熔化各种钠的化合物 |
| D.某溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
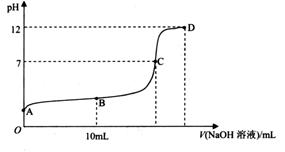
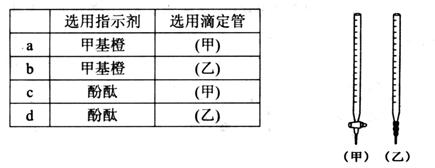
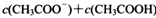 ________
________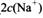 (选填“>”、“<”或“=”);
(选填“>”、“<”或“=”);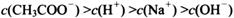
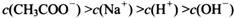
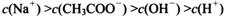
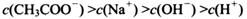
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 反应阶段 | I | II | III |
| 盐酸体积x/ mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
 是称量和 ,在实验中需要测定的数据有 。
是称量和 ,在实验中需要测定的数据有 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所用NaOH已经潮解 | B.定容时观察液面仰视 |
| C.有少量NaOH溶液残留在烧杯里 | D.称NaOH时,砝码已生锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com