
| A. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) | |
| C. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-) | |
| D. | 1.5 L 0.1 mol•L-1 NaOH溶液中缓慢通入CO2至溶液增重4.4 g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
分析 A.根据碳酸氢钠溶液中的电荷守恒判断;
B.混合液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知c(X-)>c(Na+),再结合物料守恒判断各离子浓度大小;
C.根据混合液中的电荷守恒判断;
D.增重的4.4g为二氧化碳的质量,物质的量为0.1mol,发生反应CO2+NaOH=NaHCO3、CO2+2NaOH=Na2CO3+H2O,由于n(CO2):n(NaOH)=2:3,所得溶液中溶质为等浓度的Na2CO3和NaHCO3,碳酸根离子的水解程度大于碳酸氢根离子,则c(HCO3-)>c(CO32-).
解答 解:A.0.1mol•L-1NaHCO3溶液中,根据电荷守恒可知:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故A正确;
B.等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(H+)>c(OH-),根据电荷守恒可知c(X-)>c(Na+),根据物料守恒2(Na+)=c(X-)+c(HX)可得c(X-)>c(Na+)>c(HX),则溶液中离子浓度大小为:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-),故B正确;
C.0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸等体积混合所得碱性溶液中,根据电荷守恒可得:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-),故C正确;
D.向1.5 L 0.1 mol•L-1 NaOH溶液中缓缓通入CO2气体至溶液增重4.4g,则增重的4.4g为二氧化碳的质量,物质的量为0.1mol,发生反应CO2+NaOH=NaHCO3、CO2+2NaOH=Na2CO3+H2O,由于n(CO2):n(NaOH)=2:3,所得溶液中溶质为等浓度的Na2CO3和NaHCO3,碳酸根离子的水解程度大于碳酸氢根离子,则c(HCO3-)>c(CO32-),溶液中正确的离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故D错误;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒及盐的水解原理为解答关键,D为难点、易错点,需要根据反应物的量正确判断反应产物,试题培养了学生的分析、理解能力及灵活应用能力.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:解答题
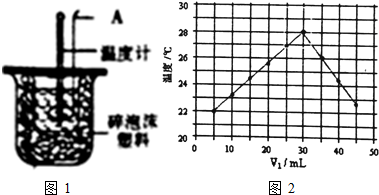 利用如图1装置测定中和热的实验步骤如下:
利用如图1装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2℃ | 温度差平均值(t2-t1)℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 1:2 | C. | 1:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
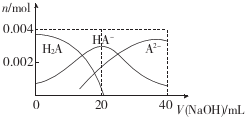
| A. | 当V(NaOH)=20 mL时,溶液中各离子浓度的大小顺序为c(Na+)>c(HA-)>c( A2-)>c( OH-)>((H+) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水中的大 | |
| C. | 等浓度H2A和NaHA的混合溶液中无论加入少量的强酸或强碱,溶液的pH变化都不大 | |
| D. | 当V(NaOH)=40 mL时,升高温度,$\frac{c(N{a}^{+})}{c({A}^{2-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
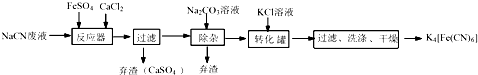
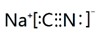 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 (g)+2NO2 (g)═N2 (g)+CO2 (g)+2H2 O(g)△H=-867 kJ•mol-1 | |
| B. | CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2O(l)△H3<△H1 | |
| C. | 若用0.2 mol CH4还原NO2至N2,则反应中放出的热量一定为173.4kJ | |
| D. | 若用标准状况下2.24 L CH4还原NO2至N2,整个过程中转移的电子为0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
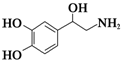
| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 1mol去甲肾上腺素分子在一定条件下可以和4molH2发生加成反应 | |
| C. | 1mol去甲肾上腺素最多能与含3mol Br2的浓溴水发生取代反应 | |
| D. | 去甲肾上腺素能与氢氧化钠溶液反应,但不能与盐酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com