
| 46g |
| 2mol |
| 22.4L |
| 22.4L/mol |
| 46g |
| 2mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
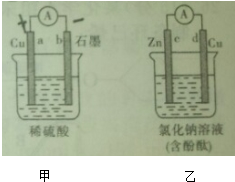
| A、甲溶液中H+的移动方向是a→b |
| B、b电极上的电极反应式为:2H++2e-═H2↑ |
| C、一段时间后,d电极附近的溶液变红 |
| D、乙装置中的溶液会逐渐变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔化时不导电 |
| B、不是离子化合物,而是极性共价化合物 |
| C、溶液中已电离的离子和未电离的分子共存 |
| D、水溶液的导电能力很差 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O
纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O
| ||
| A、钛电极发生氧化反应 |
| B、阳极附近溶液的pH逐渐增大 |
| C、离子交换膜应采用阳离子交换膜 |
| D、阳极反应式是:2Cu+2OH一一2e一═Cu2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| D、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中只含Cl2和H2O分子 |
| B、新制氯水可使蓝色石蕊试纸变红且不褪色 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后pH将变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中的氧化剂只有CuSO4 |
| B、7 mol CuSO4能氧化5mol-1价的硫 |
| C、被氧化的硫和被还原的硫个数之比是3:7 |
| D、FeS2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com