
下列装置或操作能达到实验目的的是( )
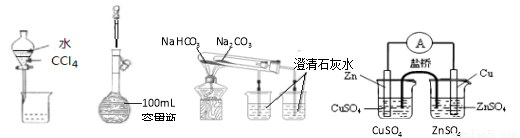
A.分离水和CCl4 B.定容
C.比较两种盐的热稳定性 D.构成铜锌原电池
 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源:2015届浙江省协作体高三第一次适应性测试理科综合化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.向Na2CO3溶液通入CO2,可使水解平衡:CO32 -+H2O HCO3- +OH-向正反应方向移动,则溶液pH增大
HCO3- +OH-向正反应方向移动,则溶液pH增大
B.室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH值
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三第一次联考化学试卷(解析版) 题型:选择题
下列表格中的各种情况,可以用下面的图象曲线表示的是
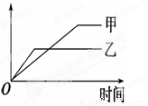
| 反应 | 纵坐标 | 甲 | 乙 |
A | 等质量的钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
B | 相同质量氨,在同一容器中2NH3 | 氨气的转化率 | 500℃ | 400℃ |
C | 在体积可变的恒压容器中,体积比1:3的N2、H2,2NH3 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2molSO2与1molO2,在相同温度下2SO2+O2 | SO3物质的量 | 10个大气压 | 2个大气压 |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期中联考化学试卷(解析版) 题型:选择题
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
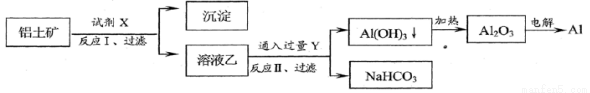
对上述流程中的判断正确的是( )
A.试剂X为稀硫酸
B.结合质子( H+)的能力由强到弱的顺序是:AlO2- > OH->CO32-
C.反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-
D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期中联考化学试卷(解析版) 题型:选择题
X、Y、Z、W四种短周期元素在周期表中的相对位置如右图所示,其中X与W的质子数之和为21,由此可知( )
| X |
| Y |
Z |
| W |
|
A.X位于元素周期表中第2周期、第VA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:填空题
(10分)如图所示的实验装置可用来测定含两种元素的某种气体X的化学式?
在注射器A中装有240 mL气体X,慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到下面的实验结果:
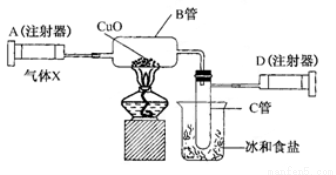
实验前B管总重20.32 g,实验后B管总重20.00 g,B管中的黑色粉末变成红色粉末?
在C管中收集到的无色液体是水;在注射器D中收集的气体是氮气?试回答下列问题:
(1)X气体是由________和________元素组成的?
(2)若240 mL X气体完全反应后,收集到的氮气质量是0.28 g?根据实验时温度和压强计算1 mol X气体的体积是24000 mL,则X的摩尔质量是________g/mol?
(3)通过计算,确定X的化学式为________?
(4)写出B中发生反应的化学方程式(X在该条件下不发生分解反应)_______________?
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:选择题
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高.则下列溶液沸点最高的是( )
A.0.01 mol/L的蔗糖溶液 B.0.01 mol/L的CaCl2溶液
C.0.02 mol/L的NaCl溶液 D.0.02 mol/L的CH3COOH溶液
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州市高三10月月考化学试卷(解析版) 题型:选择题
某碳酸钠和碳酸氢钠的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为5:4,该混合物中碳酸钠和碳酸氢钠的物质的量之比为
A.1:3 B.2:3 C.3:4 D.4:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com