
分析 (1)由相对氢气的密度计算A的分子式,再计算A、二氧化碳、水的物质的量,根据原子守恒确定有机物实验式与分子式;
(2)根据烃的分子式书写可能的结构简式;
(3)在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),结合分子式书写可能的结构简式.
解答 解:(1)二氧化碳物质的量为$\frac{22g}{44g/mol}$=0.5mol,水的物质的量为$\frac{10.8g}{18g/mol}$=0.6mol,
则烃A中C、H一直在数目之比为0.5mol:0.6mol×2=5:12,故A的实验室为C5H12,
有机物A蒸气的相对密度是相同条件下H2的36倍,则A的相对分子质量为36×2=72,则A的分子式为:C5H12,
故答案为:C5H12;C5H12;
(2)A的可能结构简式有:CH3CH2CH2CH2CH3、CH3CH2C(CH3)2、C(CH3)4,
故答案为:CH3CH2CH2CH2CH3;CH3CH2C(CH3)2;C(CH3)4;
(3)A的核磁共振氢谱中只有一个信号峰(即只有一种氢原子),A的结构简式为C(CH3)4,
故答案为:C(CH3)4.
点评 本题考查有机物的分子式确定、同分异构体书写,注意掌握燃烧法利用原子守恒确定有机物分子式,旨在考查学生对基础知识的巩固.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
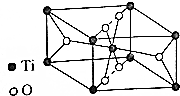 为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用.
为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用. ,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.
,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②③④⑤ | C. | ①②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
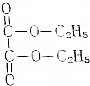 草酸二乙酯为无色油状液体,有芳香气味,主要用于医药工业中,是硫唑嘌呤、周效磺胺、羧苯脂青霉索等药物的中间体,已知它的结构如图所示:提示:
草酸二乙酯为无色油状液体,有芳香气味,主要用于医药工业中,是硫唑嘌呤、周效磺胺、羧苯脂青霉索等药物的中间体,已知它的结构如图所示:提示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ETFE极易分解,符合环保要求 | B. | ETFE韧性好,拉伸强度高 | ||
| C. | ETFE比玻璃轻、安全 | D. | ETFE是混合物,无固定的熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
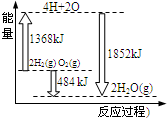
| A. | 该反应是吸热反应过程 | |
| B. | 由2molH2和1molO2变成4molH、2molO原子需要放出能量 | |
| C. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ能量 | |
| D. | 4molH、2molO生成2molH2O(g),共放出484kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| C. | S(s)+$\frac{3}{2}$O2(g)═SO3(g);△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2=O2+2NO;△H=+116.2kJ/mol(反应热) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com