
下列化学用语中,正确的是
A.氯化钠的电子式为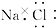
B.镁的原子结构示意图为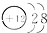
C.氯化氢分子的形成过程可用电子式表示式: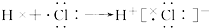
D.重水的化学式为 21H2O(或D2O)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:填空题
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子。工业上通过分离液态空气获得X单质。Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最外能层只有一个电子,其他能层均己充满电子。请回答下列问题:
(1) Z2+基态核外电子排布式为______________。
(2) YX4-的空间构型是______________,与YX4-互为等电子体的一种分子为_____________(填化学式);HYX4酸性比HYX2强,其原因是_____________。
(3)结构简式为RX (W2H3)2的化合物中R原子的杂化轨道类型为_____________;lmo1RX (W2H3) 2分子中含有σ键数目为_____________。
(4)往Z的硫酸盐溶液中通入过量的WH3,可生成[Z(WH3)4]SO4,下列说法正确的是_____________。
A. [Z(WH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(WH3)4]2+中Z2+给出孤对电子,NH3提供空轨道
C.在[Z(WH3)4]SO4组成元素中第一电离能最大的是氧元素
(5)某Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。
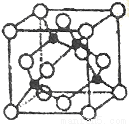
①该晶体的化学式为_____________
②已知Z和Y的电负性分别为1.9和3.0,则Y与L形成的化合物属于_____________(填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg.cm-3,阿伏加德罗常数为NA,则该晶体中Z原子和Y原子之间的最短距离为_____________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
对于锌、铜和稀硫酸构成的原电池,下列有关说法正确的是( )
①Zn是负极 ②Cu是正极
③负极反应:Zn—2e-=Zn2+ ④正极反应:Cu2++2e-=Cu
⑤H+向负极移动 ⑥电子由Cu极通过导线向Zn极移动
A.仅①②③⑤ B.①②③④⑤
C.仅②③④⑥ D.仅①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3;②Fe2O3;③Cu(NO3)2;④KNO3,铜粉溶解的是( )
A.只有①或②
B.只有②或④
C.只有①或②或③
D.上述四种物质中任意一种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
设NA表示阿伏伽德罗常数的值,下列判断正确的是
A.将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA
B.标准状况下,22.4 L甲醇中含有的C—H的数目为3NA
C.25℃时,pH=2的硫酸溶液中,含有的H+的数目为0.01NA
D.5.6 g Fe与一定量稀硝酸反应,Fe完全溶解时失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:计算题
将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3·bMn(OH)2·cH2O]。
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 ,反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 。
(2)为测定碱式碳酸锰组成,取7.390 g样品溶于硫酸,生成CO2 224.0 mL(标准状况),并配成500 mL溶液。准确量取10.00 mL该溶液,用0.0500 mol·L-1 EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2+ +H2Y2-=MnY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
下列实验目的对应的实验操作和实验原理均正确的是
实验目的 | 实验操作 | 实验原理 | |
A | 提纯混有少量硝酸钾的氯化钠 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
B | 配制FeCl3溶液 | 将FeCl3固体溶解于适量硫酸溶液 | H+抑制FeCl3水解 |
C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | NH3溶于水后溶质的主要存在形式是NH4+、OH- |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡 | 3Mg(OH)2+2Fe3+ |
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三第九次月考化学试卷(解析版) 题型:选择题
“8·12”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN)。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是____________________。
A.水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)硝酸铵在常温下比较稳定,但在强热的条件下会发生爆炸。可以得到一种无色气体和另一种红棕色的气体等物质,请写出该反应的方程式____________________;若标况下产生13mol的气体生成,则转移的电子的物质的量为________。
(3)硝酸铵和碱溶液反应生成的氨气,可以形成氨气——空气燃料电池。其反应原理为NH3+O2→N2+H2O(未配平),则电解质溶液应显____性(填“酸性”、“中性”或者“碱性”,负极的电极方程式为:______________。
(4)以TiO2为催化剂,可以用NaClO将CN-离子氧化成CNO-。在酸性条件下,NaCNO继续与NaClO反应生成N2、CO2、NaCl等。 请写出NaCNO在酸性条件下被NaClO氧化的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
下列有关同分异构体数目的叙述中,正确的是( )
A.甲苯苯环上的一个氢原子被含 4 个碳原子的烷基取代,所得产物有12种
B.等物质的量的氯气与乙烷在光照条件下反应得到10种产物
C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为6种
D.苯乙烯和氢气完全加成的产物的一溴取代物有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com