
| A. | v(B)=1.5 mol•L-1•min-1 | B. | v(B)=3 mol•L-1•min-1 | ||
| C. | v(D)=2 mol•L-1•min-1 | D. | v(C)=1 mol•L-1•min-1 |
科目:高中化学 来源: 题型:选择题
| A. | 用澄清石灰水鉴别Na2CO3和NaHCO3溶液 | |
| B. | 用焰色反应鉴别NaCl和KCl | |
| C. | 用丁达尔效应鉴别硫酸钠溶液和硅酸胶体 | |
| D. | 用排水集气法收集NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戍醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
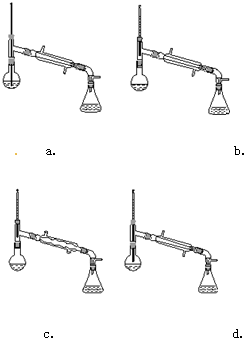
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
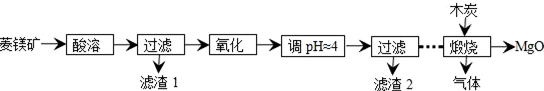

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
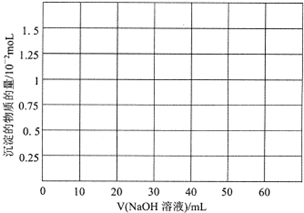
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
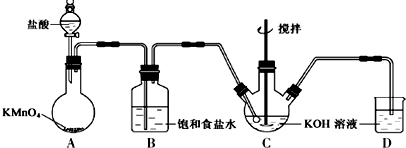
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com