
| A、淀粉、纤维素、蛋白质都是天然高分子化合物 |
| B、用于奥运“祥云”火炬的丙烷是一种清洁燃料 |
| C、用大米酿的酒在一定条件下密封保存,时间越长越香醇 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |


科目:高中化学 来源: 题型:
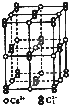 碳族元素的单质及其化合物是一类重要物质.请回答下列问题:
碳族元素的单质及其化合物是一类重要物质.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2(O2):通过灼热的镁粉 |
| B、SiO2(Fe2O3):足量的盐酸,过滤 |
| C、CO2(SO2):酸性KMnO4溶液、浓硫酸,洗气 |
| D、C2H5OH(CH3COOH):加足量CaO,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com