
| A£® | ČõĖįĖįŹ½ŃĪ NaHB ŌŚĖ®ČÜŅŗÖŠĖ®½ā£ŗHB-+H2O?H3O++B2- | |
| B£® | ¹¤ŅµÉĻµē½ā±„ŗĶŹ³ŃĪĖ®£ŗC1-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$H2”ü+Cl2”ü+OH- | |
| C£® | AlCl3ČÜŅŗÓėŠ”ĖÕ“ņČÜŅŗ»ģŗĻ£ŗAl3++3HCO3-ØTAl£ØOH£©3”ż+3CO2”ü | |
| D£® | FeBr2ČÜŅŗÖŠĶØČė¹żĮæ Cl2£ŗ2Fe2++2Br-+2Cl2ØT2Fe3++Br2+4Cl- |
·ÖĪö A£®ČõĖįĖįŹ½ŃĪĖ®½āÉś³ÉČõĖįŗĶĒāŃõøłĄė×Ó£»
B£®µē½ā±„ŗĶŹ³ŃĪĖ®Éś³ÉĒāĘų”¢ĀČĘųŗĶĒāŃõ»ÆÄĘ£»
C£®ĀĮĄė×ÓÓėĢ¼ĖįĒāøłĄė×Ó·¢ÉśĖ«Ė®½ā·“Ó¦£»
D£®ĀČĘų¹żĮ棬ŃĒĢśĄė×ÓÓėäåĄė×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2£®
½ā“š ½ā£ŗA£®HB-+H2O?H3O++B2-ĪŖµēĄė·½³ĢŹ½£¬ČõĖįĖįŹ½ŃĪ NaHB ŌŚĖ®ČÜŅŗÖŠĖ®½āµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗHB-+H2O?H2B+OH-£¬¹ŹA“ķĪó£»
B£®¹¤ŅµÉĻµē½ā±„ŗĶŹ³ŃĪĖ®µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗC1-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$H2”ü+Cl2”ü+OH-£¬¹ŹBÕżČ·£»
C£®AlCl3ČÜŅŗÓėŠ”ĖÕ“ņČÜŅŗ»ģŗĻ£¬¶žÕß·¢ÉśĖ«Ė®½ā·“Ӧɜ³ÉĒāŃõ»ÆĀĮ³ĮµķŗĶ¶žŃõ»ÆĢ¼ĘųĢ壬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAl3++3HCO3-ØTAl£ØOH£©3”ż+3CO2”ü£¬¹ŹCÕżČ·£»
D£®FeBr2ČÜŅŗÖŠĶØČė¹żĮæ Cl2£¬ŃĒĢśĄė×ÓŗĶäåĄė×Ó¶¼ĶźČ«±»Ńõ»Æ£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe2++4Br-+3Cl2ØT2Fe3++2Br2+6Cl-£¬¹ŹD“ķĪó£»
¹ŹŃ”BC£®
µćĘĄ ±¾Ģāæ¼²éĮĖĄė×Ó·½³ĢŹ½µÄŹéŠ“ÅŠ¶Ļ£¬ĪŖøßæ¼µÄøßʵĢā£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕĄė×Ó·½³ĢŹ½ÕżĪóÅŠ¶Ļ³£ÓĆ·½·Ø£ŗ¼ģ²é·“Ó¦ÄÜ·ń·¢Éś£¬¼ģ²é·“Ó¦Īļ”¢Éś³ÉĪļŹĒ·ńÕżČ·£¬¼ģ²éø÷ĪļÖŹ²š·ÖŹĒ·ńÕżČ·£¬ČēÄŃČÜĪļ”¢Čõµē½āÖŹµČŠčŅŖ±£Įō»ÆѧŹ½£¬¼ģ²éŹĒ·ń·ūŗĻŌ»Æѧ·½³ĢŹ½µČ£»ŹŌĢā²ąÖŲ»ł“”ÖŖŹ¶µÄ漲飬ӊĄūÓŚĢįøßѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2¾ßÓŠŃõ»ÆŠŌ£¬æÉÓĆÓŚĘÆ°×Ö½½¬ | |
| B£® | CO¾ßÓŠ»¹ŌŠŌ£¬æÉÓĆÓŚŅ±Į¶ĢśµČ½šŹō | |
| C£® | SiO2ČŪµćøߣ¬æÉÓĆ×÷¹āµ¼ĻĖĪ¬ | |
| D£® | Al2O3¾ßÓŠĮ½ŠŌ£¬æÉÓĆ×÷ÄĶøßĪĀ²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
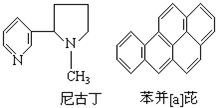
| A£® | Äį¹Å¶”ĪŖ·¼Ļć×å»ÆŗĻĪļ | |
| B£® | ±½²¢[a]ÜŵķÖ×ÓŹ½ĪŖC20H18 | |
| C£® | ±½²¢[a]ÜÅ·Ö×ÓÖŠŗ¬ÓŠ±½»·½į¹¹µ„ŌŖ£¬ŹĒ±½µÄĶ¬ĻµĪļ | |
| D£® | Äį¹Å¶”·Ö×ÓÖŠµÄĖłÓŠĢ¼Ō×ÓæÉÄܲ»ŌŚĶ¬Ņ»Ę½ĆęÉĻ£¬±½²¢[a]ÜÅ·Ö×ÓÖŠµÄĖłÓŠĒāŌ×ÓæÉÄܶ¼ŌŚĶ¬Ņ»Ę½ĆęÉĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CuS | B£® | FeS | C£® | SO3 | D£® | CuCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘųĢ¬Ēā»ÆĪļĪČ¶ØŠŌHX£¾H2Y£¾ZH3 | B£® | Ąė×Ó°ė¾¶°“X”¢Y”¢ZĖ³ŠņµŻ¼õ | ||
| C£® | µĆµē×ÓÄÜĮ¦ X£¾Y£¾Z | D£® | ĘųĢ¬Ēā»ÆĪļ»¹ŌŠŌHX£¼H2Y£¼ZH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó»ÆŗĻĪļÖŠŅ»¶Øŗ¬ÓŠĄė×Ó¼ü | |
| B£® | ÓŠ»ś¾ŪŗĻøß·Ö×ÓÖŠÖ»ŗ¬ÓŠµ„¼ü | |
| C£® | ŅŅ“¼”¢ŅŅČ©ŗĶŅŅĖį»„ĪŖĶ¬·ÖŅģ¹¹Ģå | |
| D£® | ĻĖĪ¬ĖŲŹōÓŚĢģČ»øß·Ö×Ó»ÆŗĻĪļ£¬·Ö×ÓÖŠŗ¬ÓŠĢ¼ĒāĮ½ÖÖŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ĪļÖŹIµÄ·Ö×ÓŹ½ĪŖC9H6O3 | |
| B£® | ĪļÖŹIIÖŠ“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻµÄĢ¼Ō×Ó×ī¶ąÓŠ7øö | |
| C£® | 1mol »Ŗ·ØĮÖ×ī¶ąĻūŗÄ3mol NaOH | |
| D£® | Ļņ·“Ó¦²śĪļÖŠ¼ÓČė½šŹōÄĘæɼģŃéĘäÖŠŹĒ·ńÓŠ·“Ó¦ĪļIŹ£Óą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ū¢Ż | C£® | ¢Ś¢Ū¢Ż | D£® | ¢Ś¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com