
【题目】已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
A.该溶液的pH=4
B.此酸的电离平衡常数约为1×10-7
C.升高温度,溶液的pH增大
D.由HA 电离出的c(H+) 约为水电离出的c(H+) 的106倍
【答案】C
【解析】
试题分析:HA![]() H++A-,
H++A-,
起始:0.1 0 0
变化:0.1×01% 0.1×01% 0.1×01%,
A、c(H+)=0.1×0.1%mol·L-1=10-4mol·L-1,pH=4,故说法正确;B、Ka=c(H+)×c(A-)/c(HA)=0.1×0.1%×0.1×0.1%/0.1=10-7,故说法正确;C、弱电解质的电离是吸热过程,升高温度,促进电离,即c(H+)增大,pH减小,故说法错误;D、水电离出c(H+)=c(OH-),根据水的离子积,溶液中c(OH-)=10-14/10-4=10-10,HA电离出c(H+)和水电离出c(H+)的比值为10-4:10-10=106,故说法正确。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是

A. d的氢化物比b的氢化物稳定
B. d与c不能形成化合物
C. a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a
D. 原子半径的大小顺序是a>b>c>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是
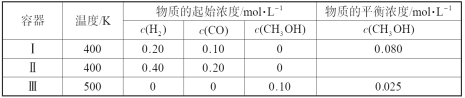
A.该反应的正反应吸热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)![]() 2NH3(g) △H2=-92.4kJ/mol ,有关数据及特定平衡状态见下表。
2NH3(g) △H2=-92.4kJ/mol ,有关数据及特定平衡状态见下表。
容器 | 起始投入 | 达平衡时 | ||
甲 | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 |
乙 | amolN2 | bmolH2 | 0molNH3 | 1.2molNH3 |
(1)若平衡后同种物质的体积分数相同,起始时乙容器通入的N2的物质的量为 ,起始时乙中的压强是甲容器的 倍,乙的平衡常数为
(2)恒容密闭容器中可以发生氨气的分解反应,达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是 (选填序号)。
a | b | c | d | |
x | 温度 | 温度 | 加入H2的物质的量 | 加入氨气的物质的量 |
y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时氨气的转化率 |
(3)研究在其他条件不变时,改变起始物氢气的物质的量对反应的影响,实验结果如图所示(图中T表示温度,n表示物质的量):
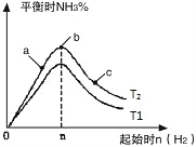
像中T2和T1的关系是:T2 T1(填“高于”“低于”“等于”“无法确定”)。
②a、b、c三点中,N2转化率最高的是 (填字母)。
③若容器容积为1L,T2℃在起始体系中加入1molN2,3molH2,经过5min反应达到平衡时H2的转化率为60%,则NH3的反应速率为 。保持容器体积不变,若起始时向容器内放入2molN2和6molH2,达平衡后放出的热量为Q,则Q_________110.88kJ(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池与现代人的生活密切相关,某同学为了研究原电池原理设计了如图所示的装置。下列说法错误的是

A. X、Y不用导线连接时,铜棒上会有银析出
B. X和Y用导线连接时,银棒上发生的电极反应为Ag++e-==Ag
C. X和Y用导线连接时,电子由银经导线移向铜,再经电解质溶液移向银
D. 无论X和Y是否用导线连接,铜棒均会溶解,溶液都从无色逐渐变成蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以黄铜矿和硫磺为原料制取钢和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
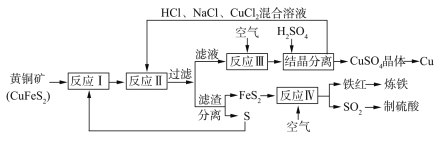
已知:“反应Ⅱ”的离子方程式为Cu2++CuS+4Cl-=2[CuCl2]-+S
回答下列问题:
(1)铁红的化学式为________;
(2)“反应Ⅱ”的还原剂是________(填化学式);
(3)除CuS外“反应II”的产物还有_________(填化学式);
(4)“反应Ⅲ”的离子方程式为_________;
(5)某同学设想利用电化学原理实现以CuSO4、SO2为原料制备Cu和H2SO4,并吸收炼铁过程中产生的CO尾气,实现资源与能源的综合利用。该同学据此组装出的装置如下图所示:
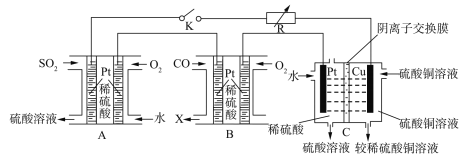
闭合该装置中的K,A池中通入SO2的Pt电极的电极反应式为__________,B池中生成的气体X的电子式为________,若在C池中生成64gCu,则整个装置中共生成H2SO4_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某饱和一元醛发生银镜反应可得21.6g银;将等量的该醛完全燃烧,生成3.6g水。此醛可能是( )
A. 甲醛 B. 乙醛 C. 丙醛 D. 丁醛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com