
为什么Na容易形成+1价离子,而Mg、Al易形成+2价、+3价离子?
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
已知Na2S2O3在中性或碱性条件下稳定,在酸性条件下会变黄,用离子方程式表示变黄的原因:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可以由下列反应合成三聚氰胺:CaO+3C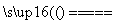 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2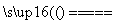 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____________________________________________。
CaCN2中阴离子为CN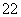 ,与CN
,与CN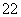 互为等电子体的分子有N2O和________(填化学式),由此可以推知CN
互为等电子体的分子有N2O和________(填化学式),由此可以推知CN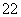 的空间构型为________。
的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________。
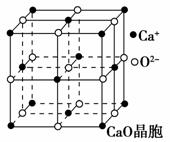 (3)三聚氰胺(
(3)三聚氰胺(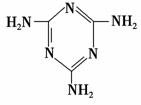 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(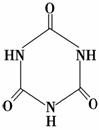 )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________。CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是__________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.周期表中的主族都有非金属元素
B.周期表中的主族都有金属元素
C.周期表中的非金属元素都位于短周期
D.周期表中的过渡元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为__________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为________,C的元素符号为________。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________,其基态原子的电子排布式为_________________________________________________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子的电子排布式为__________________________________。
(5)F元素的原子最外层电子排布式为nsnnpn+1,则n=________;原子中能量最高的是________电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是短周期元素。A的原子核外有两个电子层,最外层已达到饱和。B位于A元素的下一周期,最外层的电子数是A最外层电子数的1/2。C的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同。D与C属同一周期,D原子的最外层电子数比A的最外层电子数少1。
(1)根据上述事实判断:A是________,B是________,C是________,D是________。
(2)C的离子的核外电子排布式为________________;D原子的核外电子排布式为______________。
(3)B位于第________周期________族,它的最高价氧化物的化学式是__________,最高价氧化物的水化物是一种________酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
四种元素中的第一电离能最小的是__________,电负性最大的是__________。(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于1s、2s、3s、4s原子轨道的说法,正确的是 ( )
A.电子只能在电子云轮廓图中运动
B.轨道不同,电子云轮廓图形状相同
C.轨道数目相同,电子云轮廓图形状、大小完全相同
D.能层不同,电子云轮廓图形状也不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
为缓解能源紧张,越来越多的国家开始重视生物质能源(利用能源作物和有机废料,经过加工转变为生物燃料的一种能源)的开发利用。
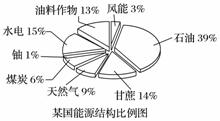
(1)如图是某国能源结构比例图,其中生物质能源所占的比例是______。
(2)生物柴油是由动植物油脂转化而来,其主要成分为脂肪酸酯,几乎不含硫,生物降解性好,一些国家已将其添加在普通柴油中使用。关于生物柴油及其使用,下列说法正确的是________。
①生物柴油是可再生资源 ②可减少二氧化硫的排放
③与普通柴油相比易分解 ④与普通柴油制取方法相同
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com