
下列关于某些离子的检验及结论,一定正确的是( )
A.加入稀盐酸产生无色气体,将该气体通入澄清石灰水中变浑浊,则一定有CO32﹣
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42﹣
C.加入稀硝酸无明显现象,再加入硝酸银有白色沉淀产生,则一定有Cl﹣
D.加入Na2CO3 溶液产生白色沉淀,再加盐酸,白色沉淀消失,则一定有Ba2+
科目:高中化学 来源:2015-2016学年广东省高一下期末化学试卷(解析版) 题型:填空题
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务。在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物进行相互反应,生成无毒物质;或者使用新型燃料电池作汽车动力,减少汽车尾气污染。
(1)H2或CO可以催化还原NO以达到消除污染的目的。
已知:N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ·mol-1
2H2(g) + O2(g) = 2H2O(l) △H =-571.6 kJ·mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是 。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2CO(g)+2NO(g) 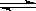 2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

① 该反应的△H 0 (填“>”或“<”)。
② 若催化剂的表面积S1>S2 ,在右图中画出c (NO) 在T1、S2 条件下达到平衡过程中的变化曲线。
(3)在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:

时间/s | 0 | 1 | 2 | 3 | 4 |
c (NO)(×10-3 mol·L-1) | 1.00 | 0.50 | 0.20 | 0.10 | 0.10 |
c (CO)(×10-3 mol·L-1) | 3.00 | 2.50 | 2.20 | 2.10 | 2.10 |
不考虑温度变化对催化剂催化效率的影响,按要求完成以下计算(写出计算过程,只写出计算结果的不给分):
①计算前2s内的△c (CO2) ;
②计算前2s内的平均反应速率v (N2) ;
③计算达到平衡时NO的转化率。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
在容积为2L的容器内,发生反应2A(s)+3B(g) 2C(g)+D(g),起始时充入3molA和2.5molB混合气体;经过5min达到平衡,生成0.5molD,下列说法正确的是( )
2C(g)+D(g),起始时充入3molA和2.5molB混合气体;经过5min达到平衡,生成0.5molD,下列说法正确的是( )
A.若单位时间内生成的B和D的物质的量之比为3:1,则体系处于平衡状态
B.C的平衡浓度为1mol/L
C.5min内B的平均消耗速率为0.3mol/(L•min)
D.平衡后,增大压强,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
粗盐中含有不溶性泥沙,可溶性的CaCl2、MgCl2以及一些硫酸盐等。精制食盐水的实验操作顺序如下:①加入过量BaCl2溶液,②加入过量NaOH溶液,③加入过量Na2CO3溶液,④过滤,⑤加入适量盐酸。下列说法不正确的是( )
A. ①②③中加入过量的试剂是为了完全除去相应的杂质离子
B. ③中加入过量Na2CO3溶液仅为了完全除去Ca2+
C. 因为Mg(OH)2难溶而MgCO3微溶,所以用NaOH除Mg2+效果比用Na2CO3好
D. ⑤中可以通过边滴加边测定溶液pH的方法,控制加入的盐酸“适量”
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
根据反应2KClO3+I2=2KIO3+Cl2↑判断,下列结论不正确的是( )
A.I2具有还原性 B.该反应属于置换反应
C.氧化剂是KClO3 D.当生成1mol Cl2时,转移2mol电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是( )
序号 | ① | ② | ③ | ④ | ⑤ |
甲 | 物质微粒数 | 标准状况下气体摩尔体积 | 固体体积 | 溶液的质量分数 | 非标准状况下物质的质量 |
乙 | 阿伏加德罗常数 | 标准状况下气体体积 | 固体密度 | 溶液的体积 | 物质的摩尔质量 |
A.②③④ B.③④⑤ C.③④ D.③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:推断题
(本题绥一高中考生不做答 ,其他考生必做)奈必洛尔是一种用于血管扩张的降血压药物。用于合成奈必洛尔中间体G的部分流程如下:
,其他考生必做)奈必洛尔是一种用于血管扩张的降血压药物。用于合成奈必洛尔中间体G的部分流程如下:
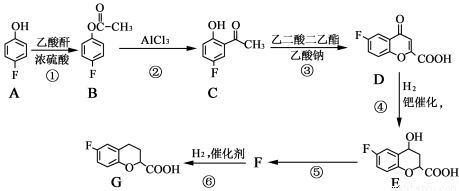
已知:乙酸酐的结构简式为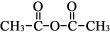
请回答下列问题:
(1)G物质中的含氧官能团的名称是 、 。
(2)反应A→B的化学方程式为 。
(3)上述④、⑤变化过程的反应类型分别是 、 。
(4)写出满足下列条件的C的一种同分异构体的结构简式:
Ⅰ.苯环上只有两种取代基。
Ⅱ.分子中只有4种不同化学环境的氢。
Ⅲ.能与NaHCO3反应生成CO2。
(5)根据已有知识并结合相关信息,写出以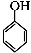 和乙酸酐为原料制备
和乙酸酐为原料制备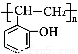 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:填空题
(1)现有反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H>0,如图表示反应II在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,则图中t2时刻发生改变的条件可能是 。
CO(g)+H2O(g) △H>0,如图表示反应II在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,则图中t2时刻发生改变的条件可能是 。
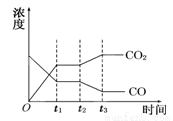
A升高温度 B降低温度 C加入催化剂 D增大压强
E减小压强 F充入CO2 G分离出部分CO
(2)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H<0
2CO2(g)+N2(g) △H<0
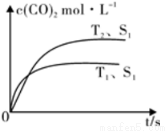
在恒容密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列反应合成甲醇:
反应I:CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
①下表所列数据是反映I在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H1 (填“>”“=”或“<”)。
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,请用三段式计算平衡常数并计算此时的温度。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:选择题
在相同温度时100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
A.中和时所需NaOH的量 B.电离度
C.H+的物质的量浓度 D.CH3COOH的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com