
【题目】在一定温度下,下列叙述是可逆反应A(g)+3B(g)![]() 2C(g)在定容密闭容器中达到平衡的标志的是
2C(g)在定容密闭容器中达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间内amol A生成,同时生成3amol B;
③A、B、C的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦A、B、C的分子数目比为1:3:2;
⑧混合气体的密度不再变化。
A. ②⑤ B. ①③④⑤ C. ②⑥⑦⑧ D. ⑤⑥⑧
【答案】B
【解析】
①C的生成速率与C的分解速率相等,即正逆反应速率相等,达到平衡状态,故①正确;②单位时间内amolA生成,同时生成3amolB只能说明单方向A、B关系,不能说明正逆反应速率的关系,故错误;③A、B、C的浓度不再变化,说明达到了平衡状态,故③正确;④因该反应是物质的量在减少的化学反应,物质的量与压强成正比,则混合气体的压强不随时间的变化而变化,达到平衡状态,故④正确;⑤混合气体的平均摩尔质量=![]() ,质量是守恒的,物质的量只有达到平衡时才不变,当混合气体的平均摩尔质量不再变化,证明达到了平衡状态,故⑤正确;⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2是反应进行到任何时刻都成立的关系,不能说明达到了平衡,故⑥错误;⑦A、B、C的分子数目比为1:3:2不是平衡大判据,故⑦错误;故选B。
,质量是守恒的,物质的量只有达到平衡时才不变,当混合气体的平均摩尔质量不再变化,证明达到了平衡状态,故⑤正确;⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2是反应进行到任何时刻都成立的关系,不能说明达到了平衡,故⑥错误;⑦A、B、C的分子数目比为1:3:2不是平衡大判据,故⑦错误;故选B。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
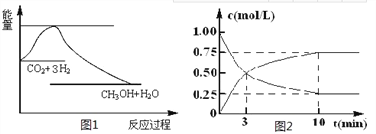
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=_________;
②下列措施中能使化学平衡向正反应方向移动的是___________(填字母)。
A.升高温度B.将CH3OH(g)及时液化抽出C.选择高效催化剂D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:_____________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极的电极反应式是:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,下列物质中最好选用
A. Cl2水 B. H2O2溶液 C. KMnO4溶液 D. HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3 , 非电解质)在空气中能发生缓慢氧化,生成剧毒物质光气(COCl2 , 非电解质),化学方程式为2CHCl3+O2=2COCl2+2HCl.检验氯仿是否被氧化应选用的试剂是( )
A.水
B.NaOH溶液
C.酚酞溶液
D.硝酸酸化的硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 对平衡体系H2(g)+I2(g)![]() 2HI(g)加压后,混合气体的颜色加深
2HI(g)加压后,混合气体的颜色加深
B. 用稀盐酸洗涤AgCl沉淀比用等体积的蒸馏水洗涤损失的AgCl少
C. 实验室可用排饱和食盐水的方法收集氯气
D. 工业合成三氧化硫的过程中使用过量的氧气,以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
(1)当空燃比(空气与燃油气的体积比)不同时,汽车尾气的主要成分不同。空燃比较小时的有毒气体主要是________(填化学式)。
(2)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。

步骤③转化反应的离子方程式是________________。按上图反应机理,NH3脱除NO、NO2总反应的化学方程式是_____________________________。
(3)NaClO2溶液将NO转化为HNO3的反应历程如下:
NaClO2+HCl===HClO2+NaCl
8HClO2===6ClO2↑+Cl2↑+4H2O
2NaClO2+Cl2===2NaCl+2ClO2↑
5NO+3ClO2+4H2O===5HNO3+3HCl
则酸性条件下NaClO2溶液将NO转化为HNO3的总反应的化学方程式为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com