
| A. | 2-甲基丁烷和异戊烷 | B. | 分子量相同而结构不同的两种物质 | ||
| C. |  和 和 | D. |  和 和 |
分析 同分异构体是指分子式相同、结构不同的化合物,注意相对分子质量相同的两种化合物,不一定具有相同的分子式,据此进行判断.
解答 解:A.2-甲基丁烷和异戊烷分子式相同,甲基都位于2号碳原子上,二者结构相同,为同一物质,故A错误;
B.分子量相同而结构不同的两种物质,它们的分子式不一定相同,如甲酸与乙醇,则不一定互为同分异构体,故B错误;
C.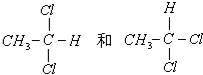 ,甲烷为四面体构型,则二氯甲烷不存在同分异构体,二者为同一物质,故C错误;
,甲烷为四面体构型,则二氯甲烷不存在同分异构体,二者为同一物质,故C错误;
D. 合
合 的分子式相同,侧链烷烃的连接方式不同,二者互为同分异构体,故D正确;
的分子式相同,侧链烷烃的连接方式不同,二者互为同分异构体,故D正确;
故选D.
点评 本题考查同分异构体的判断,题目难度不大,明确同分异构体的概念及判断方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题


 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 在水中溶解性 |
| 甲苯 | -95 | 110.6 | 0.8669 | 难溶 |
| 苯甲酸钾 | 121.5~123.5 | 易溶 | ||
| 苯甲酸 | 122.4 | 248 | 1.2659 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、H+、Cl- | B. | Na+、CO32-、Cl- | C. | Na+、H+、Cl- | D. | Na+、OH-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2═4Fe3++6Cl-+Br2 | |
| B. | 磁性氧化铁溶于氢碘酸:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| C. | 放置在空气中的淀粉碘化钾溶液一段时间后溶液呈蓝色:4H++4I-+O2═2I2+2H2O | |
| D. | 向硝酸铵溶液中滴加NaOH溶液:NH4++OH-═NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量BaCl2溶液后过滤 | B. | 加入适量NaOH溶液后过滤 | ||
| C. | 加入过量NaOH溶液后过滤 | D. | 加入过量Ba(OH)2溶液后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com