
| A. | NaCl溶液 | B. | 蔗糖 | C. | BaSO4 | D. | 铜 |
分析 电解质是:在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
非电解质是:在水溶液里和熔融状态下都不能导电的化合物,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);
单质和混合物既不是电解质也不是非电解质.
解答 解:A.氯化钠溶液属于混合物,既不是电解质也不是非电解质,故A错误;
B.蔗糖在水溶液里和熔融状态下都不能导电的化合物,是非电解质,故B错误;
C.BaSO4融状态下能导电的化合物是电解质,故C正确;
D.铜是单质,既不是电解质也不是非电解质,故D错误;
故选:C.
点评 本题考查了电解质的判断,熟悉电解质、非电解质定义是解题关键,注意单质和混合物既不是电解质也不是非电解质,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从反应开始到建立平衡所需时间:tA>tB | |
| B. | 平衡时I2的浓度:c(I2)A=c(I2)B | |
| C. | 平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器 | |
| D. | 平衡时HI的分解率:aA=aB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl+NaOH═NaCl+H2O | B. | SO3+H2O═H2SO4 | ||
| C. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
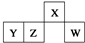 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:rW>rZ>rY>rX | |
| B. | 含Y元素的硫酸盐溶液可以和强酸、强碱反应 | |
| C. | 最简单气态氢化物的热稳定性:Z>W | |
| D. | X的氢化物与X的最高价氧化物对应的水化物能形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠钾合金可用于中子反应堆作热交换剂 | |
| B. | 氯气本身有毒,因此不能用于药物合成 | |
| C. | 不用氧化镁电解熔融制镁的原因是氧化镁不导电 | |
| D. | 工业高炉炼铁过程中,加石灰石主要是为了制备还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3产生的CO2多 | |
| B. | 等物质的量的盐酸分别与足量的Na2CO3和NaHCO3反应,Na2CO3产生的CO2多 | |
| C. | 相同温度在水中的溶解度:Na2CO3大于NaHCO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,消耗盐酸的量一样多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com