
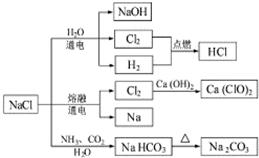
 NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的小 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下液氯能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
分析 A.由转化可知,氯化钠溶液与氨气、二氧化碳反应析出碳酸氢钠;
B.发生2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,只有Cl元素的化合价变化;
C.铁能在氯气中燃烧生成棕黄色的烟FeCl3,与干燥的氯气不反应;
D.含元素的化合价的反应为氧化还原反应.
解答 解:A.由转化可知,氯化钠溶液与氨气、二氧化碳反应析出碳酸氢钠,则25℃时,NaHCO3在水中的溶解度比Na2CO3的小,故A正确;
B.2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O中,Cl元素的化合价既升高又降低,所以Cl2既是氧化剂,又是还原剂,故B正确;
C.Fe与干燥的氯气不反应,则常温下液氯能用钢瓶贮存,但3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故C错误;
D.氯化钠和水、氨气、二氧化碳的反应以及碳酸氢钠的分解反应中均没有元素的化合价变化,则不是氧化还原反应,故D错误.
故选AB.
点评 本题考查物质的性质及相互转化,为高频考点,把握图中转化发生的反应及氧化还原反应的应用为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
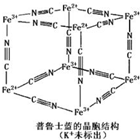 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )| A. | 化学式可以表示为KFe2(CN)6 | |
| B. | 每一个立方体中平均含有24个π键 | |
| C. | 普鲁士蓝不属于配位化合物 | |
| D. | 每个Fe3+周围与之相邻的Fe2+离子有12个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和NaHCO3 | B. | Na2CO3和NaCl | C. | Na2CO3和盐酸 | D. | NaHCO3和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子外围电子排布为msnmpn+2 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
| F | 基态F+各能级电子全充满 |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al、Mg、Na | B. | Mg、Al、Na | C. | Na、Mg、Al | D. | Na、Al、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 尽管NO2能与水反应生成硝酸,但 NO2不属于酸性氧化物 | |
| B. | Na2O 溶于水所得溶液能导电,据此可判断 Na2O属于电解质 | |
| C. | 氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应 | |
| D. | 某气体只含N、H 两种元素,且质量之比为14:3,则该气体一定为纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L苯中含有C-H键的数目为3NA | |
| B. | 常温下,1.0LPH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com