
在一定条件下进行如下反应:aX(g)+bY(g) cZ(g)。下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。
cZ(g)。下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。

(1)写出该反应的化学平衡常数表达式:K=________。随着温度的升高,K值________(填“增大”“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明________(填字母)。
A.X的转化率越高
B.反应进行得越完全
C.达到平衡时X的浓度越大
D.化学反应速率越快
(2)如图所示,相同温度下,在甲、乙两容器中各投入1molX、2molY和适量催化剂,甲、乙两容器的初始体积均为1L。甲、乙容器达到平衡所用时间:甲________乙(填“>”“<”或“=”,下同),平衡时X和Y的转化率:甲________乙。

 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:2016届安徽省高三上学期期中测试化学试卷(解析版) 题型:选择题
下列与金属腐蚀有关的说法正确的是

A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu—Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn—MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省台州市高一上学期第一次月考化学试卷(解析版) 题型:选择题
气体的体积主要由以下什么因素决定的
①气体分子的直径 ②气体物质的量的多少 ③气体分子间的平均距离 ④气体分子的相对分子质量
A.①② B.①③ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省高一上学期期中测试化学试卷(解析版) 题型:推断题
现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液.相应过程用如图表示:

(1)写出下列物质的化学式X__________;
(2)写出步骤③涉及到的离子反应__________,__________;
(3)按此实验方案得到的溶液3中肯定含有杂质,为了解决这个问题,可以向溶液3中加入适量的__________(填化学式),之后若要获得固体NaNO3需进行的实验操作是__________(填操作名称).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(1)常温下,0.2 mol·L-1HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,则
①混合溶液中由水电离出的c(H+) (填“>”、“<” 或“=”)原HCl溶液中由水电离出的c(H+)。
②求出混合溶液中下列算式的精确计算结果(填具体数字)。c(Cl-)-c(M+)= mol·L-1;
(2)常温下,若将0.2 mol·L-1MOH溶液与0.1 mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下,MOH的电离程度 (填“大于”、“小于”或“等于”) MCl的水解程度。
(3)常温下,若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH (填“>7”或“< 7”或“无法确定”)。
(4)AgNO3的水溶液呈 (填“酸”、“中”或“碱”)性,原因是(用离子方程式表示) ;实验室在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后用蒸馏水稀释到所需的浓度,以 (填“促进”或“抑制”)其水解。
(5)把FeCl3溶液蒸干、灼烧,最后得到的固体产物主要是 。
查看答案和解析>>
科目:高中化学 来源:2016届北京市高三上学期期中测试化学试卷(解析版) 题型:选择题
球墨铸铁中含有一种铁碳化合物X。实验室测定化合物X的组成实验如下:
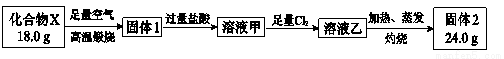
下列说法不正确的是
A.固体2是氧化铁
B.X的化学式可以表示为Fe3C2
C.溶液甲中可能含有Fe3+
D.X与足量的热浓硝酸反应有NO2和CO2生成
查看答案和解析>>
科目:高中化学 来源:2016届宁夏大学附属中学高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
(1)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛地开发和应用前景。反应:
① 下表所列数据是反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1__________0(选填“>”“=”或“<”),根据该反应特点,此反应自发进行的条件是____________(选填“高温”“低温”或“任何温度”)
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为___________。
(2)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160。此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度见下表。
物质 | H2 | CO | CH3OH |
浓度/mol·L-1 | 0.2 | 0.1 | 0.4 |
①比较此时正、逆反应速率的大小:v正__________v逆(选填“>”“<”或“=”)
②若其他条件不变,在T2℃反应10min后达到平衡,c(H2)=0.4mol·L-1,则该时间内反应速率v(CH3OH)=_____________。
(3)已知:
Al和FeO发生铝热反应的热化学方程式是 。
(4)已知:常温下,Ksp[Fe(OH)3]=4.0×10-38;当溶液的pH=4时, 则此溶液中Fe3+的物质的量浓度是_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省龙海市高二上学期期中测试化学试卷(解析版) 题型:填空题
(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式:________________________,已知 H2O(l) = H2O(g) ΔH = +44 kJ·mol-1 ,则标准状况下33.6 L H2 生成液态水时放出的热量是 kJ 。
(2)已知反应:H2(g)+ O2(g)==H2O(g) △H1
O2(g)==H2O(g) △H1
N2(g)+2O2==2NO2(g) △H2
 N2(g)+
N2(g)+ H2(g)==NH3(g) △H3
H2(g)==NH3(g) △H3
利用上述三个反应,计算4NH3(g)+7O2(g)==4NO2(g)+6H2O(g)的反应焓变为__________________(用含△H1、△H2、△H3的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.已知N2(g)+3H2(g) 2NH3(g) △H=﹣92.4kJ•mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ•mol﹣1
2NH3(g) △H=﹣92.4kJ•mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ•mol﹣1
B.1mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数NA个
C.7.8gNa2O2与过量水反应转移电子数为0.1NA
D.由1mol CH3COONa和 少量CH3COOH形成的中性溶液中,CH3COO﹣数目为NA个
少量CH3COOH形成的中性溶液中,CH3COO﹣数目为NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com