
下列将饱和碘水中的碘单质分离出来的实验操作说法正确的是
A.使用萃取的方法,并选用酒精作萃取剂
B.萃取使用的主要仪器是分液漏斗,在使用前要先检验其是否漏液
C.分液操作时,下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一烧杯中
D.从分液漏斗中分离出的就是纯净的碘单质
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年江苏省高一上期中化学试卷(解析版) 题型:选择题
相同条件下,等物质的量的两种气体一定满足
A.体积均为22.4 L B.具有相同的体积
C.是双原子组成的分子 D.所含原子数目相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南郸城高级中学高二上第二次考试化学卷(解析版) 题型:选择题
在一固定容积的密闭容器中充入2molA和1molB,发生反应2A(g)+B(g) xC(g),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB、1.4molC为起始物质,达到平衡后,C的体积分数也为W%,则x值为( )
xC(g),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB、1.4molC为起始物质,达到平衡后,C的体积分数也为W%,则x值为( )
A.1 B.2 C.3 D.2或3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州贵阳花溪清华中学高一上月考一化学卷(解析版) 题型:填空题
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
回答下列问题:
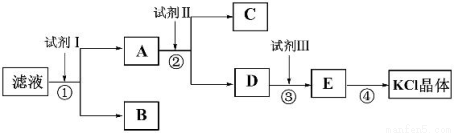
(1)①中发生反应的化学方程式为__________。
(2)②中加入试剂Ⅱ的目的是__________。
(3)操作④为蒸发,蒸发的作用之一是得到KCl晶体,另一作用是__________。
(4)某同学称取提纯的产品0.76g,溶解后定容在100mL容量瓶中,取25.00mL溶液,与25.00mL浓度为0.1000mol/L的硝酸银溶液恰好完全反应,则该产品的纯度为__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州贵阳花溪清华中学高一上月考一化学卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.标况下,1mol水分子占有的体积为22.4L
B.17gOH-中质子总数比电子总数多NA
C.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-的数目为NA
D.4g氦气中所含氦原子的数目为NA
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江大庆实验中学高三上期中化学卷(解析版) 题型:推断题
框图中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。
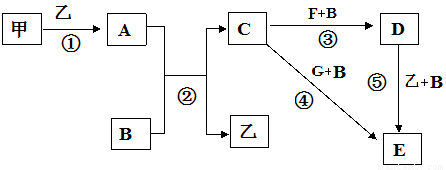
请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是______________(填序号)。
(2)反应⑤的化学方程式为____________________________。
(3)甲与B反应的离子方程式 _______________________________。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是______________________。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:__________________ 。
。
(6)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和50g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去(假设过程中液体体 积不变)。
积不变)。
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的,上述观点是否正确 。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的,设计实验证明烧瓶内溶液中含H2O2,简述实验方法 。
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江大庆实验中学高三上期中化学卷(解析版) 题型:选择题
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
A. 元素X分别与Y、Z、R可以形成多种二元共价化合物
B. 元素Y、Z、R形成的化合物的水溶液可能呈酸性、碱性或者中性
C. 热稳定性:XmY强于XmR,沸点:XmY高于XmR
D. 五种元素的单质在常温下有两种是气态、两种是固态、一种是液态
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上期中化学试卷(解析版) 题型:选择题
利用1L 3mol· L-1的盐酸、1L 3mol· L-1的氢氧化钠溶液和足量的铝单质,最多可以制备得到氢氧化铝的物质的量为
A.1mol B.3mol C.4mol D.6mol
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学卷(解析版) 题型:选择题
某磁黄铁矿的主要成分是FexS(S为﹣2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成硫单质2.4g、FeCl2 0.425mol和一定量H2S气体,且溶液中无Fe3+.则下列说法正确的是
A.100mL的盐酸中HCl物质的量浓度为7.5mol/L
B.生成的H2S气体在标准状况下的体积为2.24L
C.该磁黄铁矿中FexS的x=0.85
D.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com