
【题目】实验室模拟由“侯氏制碱法”制取Na2CO3,以下实验步骤能实现的是( )
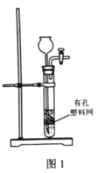

A.用图1装置由石灰石与稀盐酸制备CO2
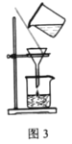
B.用图2装置除去CO2中的HCl
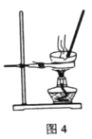
C.用图3装置过滤所得的NaHCO3固体
D.用图4装置加热灼烧NaHCO3固体制Na2CO3
科目:高中化学 来源: 题型:
【题目】某学习小组欲根据侯德榜制碱的原理制备少量纯碱。下列实验步骤对应的实验装置(夹持装置已略去)和相关解释或说明均正确的是( )
选项 | A | B | C | D |
实验步骤 | 制备NH3 | 制备NaHCO3 | 分离NaHCO3 | 煅烧NaHCO3 |
实验装置 |
|
|
|
|
解释或说明 | 试剂X可选择NH4Cl | 从a口通入足量NH3,再从b口通入足量CO2,可增大产品的产率 | 该装置可用于分 离NaHCO3 | 无水CuSO4的作用是检验NaHCO3是否完全分解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在氨水中存在下列平衡:NH3+H2O![]() NH3H2O
NH3H2O![]() NH
NH![]() +OH-。
+OH-。
(1)向氨水中加入MgCl2固体时,平衡向__移动,OH-离子的浓度__,NH![]() 离子的浓度__;
离子的浓度__;
(2)向氨水中加入浓盐酸,平衡向__移动,此时溶液中浓度减小的微粒有__、__、__;
(3)向浓氨水中加入少量的NaOH固体,平衡向__移动,此时发生的现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将V mL 0.10mol·L-1的NaOH溶液逐滴滴入到20.00mL 0.10mol·L-1的醋酸溶液中,溶液pH随所加V(NaOH)的变化而变化(忽略混合时溶液体积变化),数据如下表所示:

下列说法正确的是
A.①中存在c(CH3COO-)>c(Na+)=0.05mol·L-1
B.②中存在c(CH3COOH)<c(Na+)=c(CH3COO-)=x /(200+10x)
C.③中存在c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.05mol·L-1
D.通过①进行近似计算可知醋酸的数量级是10-6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
(1)硫酸铜溶液可以加快氢气生成速率的原因是____。
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
实验序号 | 体积/mL | ||
1.0mol·L-1硫酸溶液 | 饱和CuSO4溶液 | 水 | |
I | 30.0 | 1.0 | 9.0 |
II | 20.0 | 1.0 | Vx |
III | 30.0 | 3.0 | 7.0 |
①本实验待测数据可以是____。
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=__,理由是__。
③实验I和实验III的目的是__。
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 60 | 140 | 252 | 420 | 510 | 540 |
①反应速率最大时间段是__min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”或“5~6”下同),原因是____。
②反应速率最小时段是__min,原因是___。
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=___。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是____(填字母)。
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答
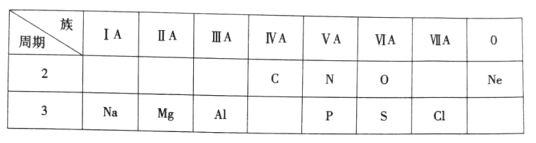
(1)镁元素位于元素周期表中第___周期_____族;
(2)空气组成中体积分数最大的气体是_____;
(3)O与S相比,原子半径较小的是____;
(4)金刚石的组成元素是________;
(5)单质的化学性质最不活泼的元素是______;
(6)Na与Mg元素相比金属性较强的是_________
(7)NH3与PH3相比,热稳定性较弱的是______
(8)H2SO4与H3PO4相比酸性较强的是______
(9)Mg(OH)2与Al(OH)3其中属于两性氢氧化物的是________
(10)单质呈黄绿色的气体组成元素是_____,其单质的水溶液呈__(填“酸性或“碱性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟用![]() 溶液和
溶液和![]() 溶液混合制备
溶液混合制备![]() ,再将所得
,再将所得![]() 与
与![]() 溶液混合,可制备草酸合铜酸钾晶体
溶液混合,可制备草酸合铜酸钾晶体![]() 。通过下述实验确定该晶体的组成。
。通过下述实验确定该晶体的组成。
步骤Ⅰ 称取![]() 样品,放入锥形瓶,加入适量
样品,放入锥形瓶,加入适量![]() 稀硫酸,微热使样品溶解,再加入
稀硫酸,微热使样品溶解,再加入![]() 水加热,用
水加热,用![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液。
溶液。
步骤Ⅱ 将步骤Ⅰ的溶液充分加热,使淡紫红色消失,溶液最终显示蓝色。冷却后,调节![]() 并加入过量
并加入过量![]() 固体,与
固体,与![]() 反应生成
反应生成![]() 沉淀和
沉淀和![]() ,以淀粉作指示剂,用
,以淀粉作指示剂,用![]() 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗![]() 标准溶液。
标准溶液。
已知:![]() ;
;
![]() ;
;![]()
回答下列问题:
(1)室温下,![]() ,
,![]() ,
,![]() 溶液
溶液![]() ________7(填“>”或“<”或“=”)。
________7(填“>”或“<”或“=”)。
(2)步骤Ⅱ中滴定终点的现象为________。
(3)步骤Ⅱ中若消耗的![]() 标准溶液的体积偏大,可能的原因有________(填字母)。
标准溶液的体积偏大,可能的原因有________(填字母)。
A.滴定前未将待测溶液充分加热
B.锥形瓶水洗后未干燥
C.装![]() 标准溶液的滴定管水洗后未润洗
标准溶液的滴定管水洗后未润洗
D.滴定时锥形瓶中有液体溅出
(4)通过计算确定该晶体的化学式(写出计算过程)。
________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol/L降到0.07mol/L,则下列说法正确的是( )
H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol/L降到0.07mol/L,则下列说法正确的是( )
A.缩小反应体系的体积,化学反应速率加快
B.c(HI)由0.07mol/L降到0.05mol/L所需的反应时间小于10s
C.升高温度正反应速率加快,逆反应速率减慢
D.0~15s内用I2表示的平均反应速率为v(I2)=0.002mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的空间构型为__ __;F2+的核外电子排布式为 。
(2)A分别与B、C形成的最简单化合物的稳定性B____C(填“大于”或“小于”);A、C两元素可组成原子个数比为1:1的化合物,C元素的杂化类型为 。
(3)A2C所形成的晶体类型为_ ___;F单质形成的晶体类型为 ,其采用的堆积方式为 。
(4)F元素氧化物的熔点比其硫化物的____(填“高”或 “低”),请解释其原因____。
(5)D跟E可形成离子化合物,其晶胞结构如右图。该离子化合物晶体的密度为pg.cm。3,则晶胞的体积是 。(用含p的代数式表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com