
已知NO2与N2O4可相互转化:2NO2(g)?N2O4(g);ΔH=-24.2 kJ/mol,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如下图所示。
下列推理分析合理的是
| A.前10 min内,用v(NO2)表示的反应速率为0.02 mol/(L·min) |
| B.反应进行到10 min时,体系吸收的热量为9.68 kJ |
| C.a、b、c、d四点中v正与v逆均相等 |
| D.25 min时,导致平衡移动的原因是升温 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 已知NO2与N2O4相互转化:2NO2(g)?N2O4(g);△H=-24.4kJ/mol
已知NO2与N2O4相互转化:2NO2(g)?N2O4(g);△H=-24.4kJ/mol| A、前10min内,用v(NO2)表示的该反应速率为0.02mol/L?min | B、反应进行到10min时,体系吸收的热量为9.76kJ | C、a,b,c,d四点中c正与v逆均相等 | D、25min时,导致平衡移动的原因是升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
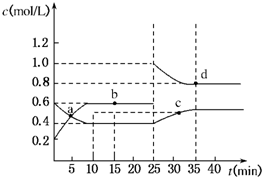 已知NO2与N2O4可相互转化:2NO2(g)?N2O4(g);△H=-24.2kJ/mol,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示.下列推理分析合理的是( )
已知NO2与N2O4可相互转化:2NO2(g)?N2O4(g);△H=-24.2kJ/mol,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示.下列推理分析合理的是( )| A、反应进行到10 min时,体系吸收的热量为9.68 kJ | B、前10 min内,用v(NO2)表示的反应速率为0.02 mol/(L?min) | C、a、b、c、d四点中v正与v逆均相等 | D、25 min时,导致平衡移动的原因是升温 |
查看答案和解析>>
科目:高中化学 来源:2013届江西省高二上学期期末联考化学试卷 题型:选择题
已知NO2与N2O4可相互转化:2NO2(g)⇌N2O4(g);ΔH=-24.2 kJ/mol,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如下图所示。下列推理分析合理的是( )

A. 反应进行到10 min时,体系吸收的热量为9.68 kJ
B. 前10 min内,用v(NO2)表示的反应速率为0.02 mol/(L·min)
C.a、b、c、d四点中v正与v逆均相等
D.25 min时,导致平衡移动的原因是升温
查看答案和解析>>
科目:高中化学 来源:2013届广西武鸣高中高二上学期段考化学(理)试卷 题型:选择题
已知NO2与N2O4可相互转化:2NO2(g)⇌N2O4(g);ΔH=-24.2 kJ/mol,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如下图所示。

下列推理分析合理的是
A. 前10 min内,用v(NO2)表示的反应速率为0.02 mol/(L·min)
B. 反应进行到10 min时,体系吸收的热量为9.68 kJ
C. a、b、c、d四点中v正与v逆均相等
D. 25 min时,导致平衡移动的原因是升温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com