
”¾ĢāÄæ”æŌŚt”ćCŹ±£¬AgBrŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ÓÖÖŖt”ćCŹ±AgClµÄKsp=4”Į10©10 £¬ ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£© 
A.Ķ¼ÖŠaµć¶ŌÓ¦µÄŹĒAgBrµÄ²»±„ŗĶČÜŅŗ
B.ŌŚt”ćCŹ±£¬AgBrµÄKspĪŖ 4.9”Į10©13
C.ŌŚAgBr±„ŗĶČÜŅŗÖŠ¼ÓČėNaBr¹ĢĢ壬æÉŹ¹ČÜŅŗÓÉcµćµ½bµć
D.ŌŚt”ćCŹ±£¬AgCl£Øs£©+Br©£Øaq£©AgBr£Øs£©+Cl©£Øaq£©µÄĘ½ŗā³£ŹżK”Ö816
”¾“š°ø”æC
”¾½āĪö”æ½ā£ŗA£®aµćŌŚĒśĻßµÄĻĀ·½£¬c£ØBr©£©c£ØAg+£©£¼Ksp£ØAgBr£©£¬¶ŌÓ¦µÄŹĒAgBrµÄ²»±„ŗĶČÜŅŗ£¬¹ŹAÕżČ·£»
B£®t”ćCŹ±£¬cµćKsp=c£ØBr©£©c£ØAg+£©=7”Į10©7”Į7”Į10©7=4.9”Į10©13£¬¹ŹBÕżČ·£»
C£®ŌŚAgBr±„ŗĶČÜŅŗÖŠ¼ÓČėNaBr¹ĢĢ壬c£ØBr©£©Ōö“ó£¬ČܽāĘ½ŗāÄęĻņŅĘ¶Æ£¬c£ØAg+£©¼õŠ”£¬¶ųÓÉcµćµ½bµćc£ØAg+£©²»±ä£¬Ōņ²»ÄÜŹ¹ČÜŅŗÓÉcµćµ½bµć£¬¹ŹC“ķĪó£»
D£®ŌŚt”ćCŹ±£¬AgCl£Øs£©+Br©£Øaq£©AgBr£Øs£©+Cl©£Øaq£©µÄĘ½ŗā³£ŹżK= ![]() =
= ![]() =
= ![]() ”Ö816£¬¹ŹDÕżČ·£»
”Ö816£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
A£®aµćŌŚĒśĻßµÄĻĀ·½£¬c£ØBr©£©c£ØAg+£©£¼Ksp£ØAgBr£©£»
B£®t”ćCŹ±£¬cµćKsp=c£ØBr©£©c£ØAg+£©£»
C£®ŌŚAgBr±„ŗĶČÜŅŗÖŠ¼ÓČėNaBr¹ĢĢ壬c£ØBr©£©Ōö“ó£¬ČܽāĘ½ŗāÄęĻņŅĘ¶Æ£¬c£ØAg+£©¼õŠ”£»
D£®ŌŚt”ćCŹ±£¬AgCl£Øs£©+Br©£Øaq£©AgBr£Øs£©+Cl©£Øaq£©µÄĘ½ŗā³£ŹżK= ![]() =
= ![]() £®
£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”擦Ąķ¹¤ŅµĖįŠŌ·ĻĖ®ÖŠNO3-µÄµē½ā³Ų¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬µē½ā×Ü·“Ó¦ĪŖ4NO3-+4H+![]() 2N2”ü+5O2”ü+2H2O”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
2N2”ü+5O2”ü+2H2O”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
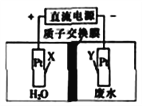
A. Xµē¼«ÉĻ·¢Éś»¹Ō·“Ó¦
B. Yµē¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖ2NO3-+10e-+12H+==N2”ü+6H2O
C. µē½ā³Ų¹¤×÷Ź±£¬H+“ÓÖŹ×Ó½»»»Ä¤ÓŅ²ąĻņ×ó²ąŅʶÆ
D. µē½ā³Ų¹¤×÷Ź±£¬µēĀ·ÖŠĆæĶعż2molµē×Ó£¬Éś³É15.68LĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠpH=2µÄ“×ĖįČÜŅŗ¼×ŗĶpH=2µÄŃĪĖįŅŅ£¬Ēėøł¾ŻĻĀĮŠ²Ł×÷Ķź³ÉĪŹĢā£ŗ
£Ø1£©Č”10mLµÄ¼×ČÜŅŗ£¬¼ÓČėµČĢå»żµÄĖ®£¬“×ĖįµÄµēĄėĘ½ŗā£ØĢī”°Ļņ×ó”±”¢”°ĻņÓŅ”±»ņ”°²»”±£©ŅĘ¶Æ£»ĮķČ”10mLµÄ¼×ČÜŅŗ£¬¼ÓČėÉŁĮæĪŽĖ®“×ĖįÄĘ¹ĢĢå£Ø¼ŁÉč¼ÓČė¹ĢĢåĒ°ŗó£¬ČÜŅŗĢå»ż±£³Ö²»±ä£©£¬“ż¹ĢĢåČÜĶźŗó£¬ČÜŅŗÖŠ ![]() µÄ±ČÖµ½«£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°ĪŽ·ØČ·¶Ø”±£©£®
µÄ±ČÖµ½«£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°ĪŽ·ØČ·¶Ø”±£©£®
£Ø2£©ĻąĶ¬Ģõ¼žĻĀ£¬Č”µČĢå»żµÄ¼×”¢ŅŅĮ½ČÜŅŗ£¬ø÷Ļ”ŹĶ100±¶£®Ļ”ŹĶŗóµÄČÜŅŗ£¬ĘäpH“󊔹ŲĻµĪŖ£ŗpH£Ø¼×£©pH£ØŅŅ£©£®£ØĢī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£¬ĻĀĶ¬£©
£Ø3£©ø÷Č”25mLµÄ¼×”¢ŅŅĮ½ČÜŅŗ£¬·Ö±šÓƵČÅØ¶ČµÄNaOHĻ”ČÜŅŗÖŠŗĶÖĮpH=7£¬ŌņĻūŗĵÄNaOHČÜŅŗµÄĢå»ż“󊔹ŲĻµĪŖ£ŗV£Ø¼×£©V£ØŅŅ£©£®
£Ø4£©Č”25mLµÄ¼×ČÜŅŗ£¬¼ÓČėµČĢå»żpH=12µÄNaOHČÜŅŗ£¬·“Ó¦ŗóČÜŅŗÖŠ[Na+]”¢[CH3COO©]µÄ“󊔹ŲĻµĪŖ£ŗ[Na+][CH3COO©]£®
£Ø5£©Č”25mLµÄŅŅČÜŅŗ£¬¼ÓČėµČĢå»żpH=12µÄ°±Ė®£¬·“Ó¦ŗóČÜŅŗÖŠµÄČÜÖŹĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ¼Č²»ŹĒµē½āÖŹ,ÓÖ²»ŹĒ·Ēµē½āÖŹµÄŹĒ
A.Ź³ŃĪĖ®B.ŅŅ“¼C.NaHSO4D.Ca(OH)2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠĶØČėĮ½ÖÖĘųĢå·¢Éś»Æѧ·“Ó¦£¬·“Ó¦ÖŠø÷ĪļÖŹ£ØA”¢B”¢C”¢D£©µÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼MĖłŹ¾£¬¶ŌøĆ·“Ó¦µÄĶʶĻŗĻĄķµÄŹĒ£Ø””””£© 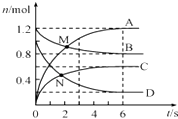
A.Mµć±ķŹ¾v£ØA£©=v£ØB£©
B.0”«6sÄŚ£¬v£ØA£©£ŗv£ØB£©£ŗv£ØC£©£ŗv£ØD£©=3£ŗ1£ŗ1.5£ŗ2
C.·“Ó¦½ųŠŠµ½6sŹ±£¬ø÷ĪļÖŹµÄĪļÖŹµÄĮæÅضČĻąµČ
D.·“Ó¦½ųŠŠµ½6sŹ±£¬CµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ 0.1molL©1s©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[»ÆѧєŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ”æ
ōä“äŹĒÓńŹÆÖŠµÄŅ»ÖÖ£¬ĘäÖ÷ŅŖ³É·ÖĪŖ¹čĖįĀĮÄĘ-NaAI(Si2O6)£¬³£ŗ¬Ī¢ĮæCr”¢Ni”¢Mn”¢Mg”¢FeµČŌŖĖŲ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
(l)»łĢ¬CrŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ____£»FeĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄ___ Ēų”£
(2)ōä“äÖŠÖ÷ŅŖ³É·Ö¹čĖįĆŖÄʱķŹ¾ĪŖŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖ____£¬ĘäÖŠĖÄÖÖŌŖĖŲµŚŅ»µēĄėÄÜÓÉŠ”µ½“óµÄĖ³ŠņŹĒ____”£
(3)øĘŗĶĢś²æŹĒµŚĖÄÖÜĘŚŌŖĖŲ£¬ĒŅŌ×ÓµÄ×īĶā²ćµē×ÓŹżĻąĶ¬£¬ĪŖŹ²Ć“ĢśµÄČŪ·ŠµćŌ¶“óÓŚøĘ£æ____”£
(4)ŌŚ¹čĖįŃĪÖŠ“ęŌŚ![]() ½į¹¹µ„ŌŖ£¬ĘäÖŠSiŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ____”£µ±ĪŽĻŽ¶ąøö£ØÓĆn±ķŹ¾£©
½į¹¹µ„ŌŖ£¬ĘäÖŠSiŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ____”£µ±ĪŽĻŽ¶ąøö£ØÓĆn±ķŹ¾£©![]() ·Ö±šŅŌ3øö¶„½ĒŃõŗĶĘäĖū3øö
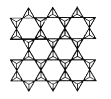
·Ö±šŅŌ3øö¶„½ĒŃõŗĶĘäĖū3øö![]() ŠĪ³É²ćד½į¹¹Ź±£ØČēĶ¼ĖłŹ¾£©£¬ĘäÖŠSi”¢OŌ×ӵďżÄæÖ®±ČĪŖ____”£
ŠĪ³É²ćד½į¹¹Ź±£ØČēĶ¼ĖłŹ¾£©£¬ĘäÖŠSi”¢OŌ×ӵďżÄæÖ®±ČĪŖ____”£
ČōĘäÖŠÓŠŅ»°ėµÄSi±»AlĢę»»£¬Ęä»ÆѧŹ½ĪŖ____”£
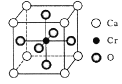
(5) CrŗĶCaæÉŅŌŠĪ³ÉÖÖ¾ßÓŠĢŲŹāµ¼µēŠŌµÄø“ŗĻŃõ»ÆĪļ£¬¾§°ū½į¹¹ČēĶ¼ĖłŹ¾”£øĆ¾§ĢåµÄ»ÆѧŹ½ĪŖ____£¬ČōCaÓėOµÄŗĖ¼ä¾ąĄėĪŖx nm£¬ŌņøĆ¾§ĢåµÄĆܶČĪŖ___ g/cm3”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ»ģŗĻĪļµÄ·ÖĄė»ņĢį“棬³£²ÉÓƵķ½·ØÓŠ£ŗ¢Ł¹żĀĖ”¢¢ŚÕō·¢”¢¢ŪÕōĮó”¢¢ÜŻĶČ””¢¢Ż¼ÓČČ·Ö½āµČ£®ĻĀĮŠø÷»ģŗĻĪļµÄ·ÖĄė»ņĢį“æÓ¦²ÉÓĆŹ²Ć“·½·Ø£æ£ØĢīŠņŗÅ£©
£Ø1£©ĢįČ”µāĖ®ÖŠµÄµā £®
£Ø2£©³żČ„Ź³ŃĪČÜŅŗÖŠµÄĖ® £®
£Ø3£©µ»Æŗ£Ė® £®
£Ø4£©³żČ„KC1¹ĢĢåÖŠŗ¬ÓŠµÄÉŁĮæKClO3 £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĪļÖŹµÄ·ÖĄąÖŠ£¬²»ŗĻĄķµÄŹĒ£Ø £©
A.NaOH£ØĒæ¼ī£©
B.CO2£ØŃõ»ÆĪļ£©
C.H2SO4£ØČõĖį£©
D.ŃĪĖį£Ø»ģŗĻĪļ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·°ŹĒŅ»ÖÖČŪµćøß”¢Ó²¶Č“ó”¢ĪŽ“ÅŠŌµÄ½šŹō£¬¹ć·ŗÓ¦ÓĆÓŚøÖĢś”¢ŗ½æÕŗ½Ģģ”¢ÄÜŌ“”¢»Æ¹¤µČĮģÓņ”£ÄæĒ°¹¤ŅµÉĻŹ¹ÓĆŅ»ÖÖŠĀ¹¤ŅÕ£¬ŅŌ±ć“ÓŅ±Į¶ĀĮµÄ¹ĢĢå·ĻĮĻŅ»³ąÄąÖŠĢįČ”½šŹō·°£¬³ąÄąÖ÷ŅŖŗ¬ÓŠFe2O3”¢Al2O3”¢V2O5ŗĶCuO£¬¾ßĢ幤ŅÕĮ÷³ĢĶ¼ČēĻĀ:
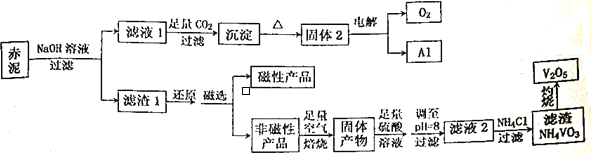
ŅŃÖŖ:·°ÓŠ¶ąÖÖ¼ŪĢ¬£¬ĘäÖŠ+5¼Ū×īĪČ¶Ø”£·°ŌŚČÜŅŗÖŠÖ÷ŅŖŅŌVO2+ŗĶVO3-µÄŠĪŹ½“ęŌŚ£¬ĒŅ“ęŌŚĘ½ŗāVO2++H2O![]() VO3-+2H+”£»Ų“šĻĀĮŠĪŹĢā:
VO3-+2H+”£»Ų“šĻĀĮŠĪŹĢā:
(1)“ÅŠŌ²śĘ·µÄ»ÆѧŹ½ĪŖ_________________________”£
(2)³ąÄą¼ÓČėNaOHČÜŅŗ£¬·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ___________________”£ÄÜ·ńÓĆ°±Ė®“śĢęNaOHČÜŅŗ£¬___________(Ģī”°ÄÜ”±»ņ”°²»ÄÜ”±)£¬ĄķÓÉŹĒ___________________________________________”£
(3)ĀĖŅŗ1Éś³É³ĮµķµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ_________________________________________”£
(4)µ÷ÖĮpH=8µÄÄæµÄÓŠĮ½øö£¬Ņ»ŹĒ___________________£¬¶žŹĒŹ¹VO2+×Ŗ»ÆĪŖVO3-£¬“ĖŹ±ČÜŅŗÖŠVO2+ŗĶVO3-µÄĪļÖŹµÄĮæÖ®±ČĪŖa:b£¬VO2++H2O![]() VO3-+2H+µÄĘ½ŗā³£ŹżK=____________________”£
VO3-+2H+µÄĘ½ŗā³£ŹżK=____________________”£
(5)ĀĖŅŗ2¼ÓĀČ»Æļ§Éś³ÉNH4VO3µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________£¬øĆ·“Ó¦ÄÜ·¢ÉśŹĒŅņĪŖ__________________________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com