

分析 (1)①次氯酸钙具有强的氧化性,能够氧化盐酸,生成氯化钙、氯气和水,依据化合价升级数目相同配平方程式;
②生成物中含有杂质氯化氢、水蒸气;装置C亦是安全瓶,监测实验进行时D中是否发生堵塞,发生堵塞时C中的压强增大,C中长颈漏斗中液面上升,形成水柱;
③可通过无水氯化钙除去水蒸气;
(2)根据固体表面积越大,反应速率越快;
(3)①蒸馏前若发现试管中液体呈黄色,说明含有氯气,可以通过氯气与锡花反应而除去;
②根据蒸馏装置应通过温度计控制温度;根据四氧化锡(SnCl4)在潮湿的空气中易水解,必须防止水的进入;
③根据收集的SnCl4中混有氯气,氯气有毒,可通过碱性溶液吸收;
解答 解:(1)①漂白粉固体和浓盐酸反应生成氯化钙、氯气和水,化学方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
故答案为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
②反应过程中氯化氢和水蒸气是氯气中的杂质,装置B中饱和食盐水的作用是除去Cl2中的HCl;装置C亦是安全瓶,监测实验进行时D中是否发生堵塞,发生堵塞时C中的压强增大,C中长颈漏斗中液面上升,形成水柱;
故答案为:除去Cl2中的HCl;长颈漏斗中液面上升,形成水柱;
③生成物中含有杂质水蒸气,可通过无水氯化钙除去水蒸气;
故答案为:无水氯化钙;
(2)用锡花代替锡粒的目的是增大与氯气的接触面积,加快反应速率;
故答案为:增大与氯气的接触面积,加快反应速率;
(3)①蒸馏前若发现试管中液体呈黄色,说明含有氯气,氯气与锡花反应,可采取的措施是加入锡花;
故答案为:加入锡花;
②蒸馏装置应通过温度计控制温度;四氧化锡(SnCl4)在潮湿的空气中易水解,必须防止水的进入;该装置汇总有两处不合理之处,它们分别是缺少温度计;Ⅱ和Ⅲ之间缺少干燥装置;
故答案为:缺少温度计;Ⅱ和Ⅲ之间缺少干燥装置;
③收集的SnCl4中混有氯气,氯气有毒,可通过氢氧化钠溶液吸收;
故答案为:氢氧化钠溶液.
点评 本题考查了氯气、四氧化锡的制备和性质,明确制备的原理和物质的性质是解题关键,注意题目信息的提取,题目难度中等.


科目:高中化学 来源: 题型:解答题
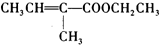 ;以化合物A为原料合成F的工艺流程如图:
;以化合物A为原料合成F的工艺流程如图:

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L | B. | 22.4L | C. | 33.6L | D. | 44.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
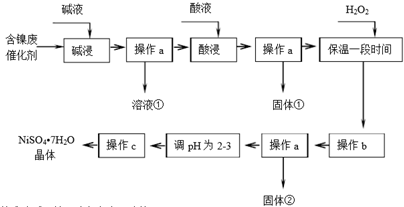
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀pH | 3.8 | 2.7 | 7.6 | 7.1 |
| 完全沉淀pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.请回答下列问题:
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.请回答下列问题:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A. | 表中①组的反应只可能有一种元素被氧化和一种元素被还原 | |
| B. | 表②中若生成标准状况下6.72LCl2,转移电子数为0.6NA | |
| C. | 由表中①②组反应推测:ClO3-、Br-、H+、Fe2+不能在浓溶液中大量共存 | |
| D. | 表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com