
ij�¶��£�H2(g)��CO2(g)? ?H2O(g)��CO(g)��ƽ�ⳣ��K��9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
?H2O(g)��CO(g)��ƽ�ⳣ��K��9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
| ��ʼŨ�� | �� | �� | �� |
| c(H2)/mol��L��1 | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol��L��1 | 0.010 | 0.010 | 0.020 |
C
��������������ÿ��淴Ӧ��������ϵ����ȣ��ں��������£��ױ�������Ϊ��Чƽ�⣬�����ʵİٷֺ�����Ӧ��ȡ����߸�����Ũ�Ⱦ�Ϊǰ�ߵ�������
��Ӧ��H2 �� CO2 H2O �� CO
H2O �� CO
��ʼ��0.01 0.01 0 0
��Ӧ x x x x
ƽ��0.01��x 0.01��x x x
��H2��Ӧ��x�������ƽ�ⳣ����֪ �����������x=0.06�����������з�Ӧ���ת����Ϊ60%�����൱�����ڼĻ���������������Ũ�ȣ����Կ������CO2��ת���ʣ�A��ȷ�����ڷ�Ӧǰ����������Dz���ģ���˼ͱ���ƽ��״̬�ǵ�Ч�ģ���ƽ��ʱ����c(CO2)��2����0.010��0.010x����0.008 mol/L��B��ȷ��C����ȷ�����з�Ӧ���Ũ�����Ӧ������죬D��ȷ����ѡC��
�����������x=0.06�����������з�Ӧ���ת����Ϊ60%�����൱�����ڼĻ���������������Ũ�ȣ����Կ������CO2��ת���ʣ�A��ȷ�����ڷ�Ӧǰ����������Dz���ģ���˼ͱ���ƽ��״̬�ǵ�Ч�ģ���ƽ��ʱ����c(CO2)��2����0.010��0.010x����0.008 mol/L��B��ȷ��C����ȷ�����з�Ӧ���Ũ�����Ӧ������죬D��ȷ����ѡC��
���㣺������淴Ӧ���йؼ��㡢ƽ��״̬���жϺ�Ӧ�á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ�в�������������ԭ�������͵���
| A����H2Sˮ��Һ�м���NaOH����������S2������ |
| B�������������������SO2ת��ΪSO3 |
| C����ѹ�Ժϳɰ����� |
| D��500 �����ұ����¸������ڰ��ĺϳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ҵ�Ͽ����úϳ�����CO��H2�Ļ�����壩�����״�����֪��
CO(g)+2H2(g) CH3OH(g) ��H=��92.9kJ/mo1
CH3OH(g) ��H=��92.9kJ/mo1
һ�������£��÷�Ӧ��һ����̶����ܱ������дﵽƽ�⡣����˵����ȷ����
| A���÷�Ӧ�ġ�S<0 |
| B���÷�Ӧ���κ��¶��¾����Է����� |
| C���������г�������He��ƽ��������Ӧ�����ƶ� |
| D�������¶�ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
NO2��������ƽ�⣺2NO2(g)  N2O4(g)+Q��Q>0�� �ڲⶨNO2����Է�������ʱ�����������²ⶨ�����ӽ�����ֵ����
N2O4(g)+Q��Q>0�� �ڲⶨNO2����Է�������ʱ�����������²ⶨ�����ӽ�����ֵ����
| A���¶�130�桢ѹǿ3.03��105 Pa | B���¶�25�桢ѹǿ1.01��105 Pa |
| C���¶�130�桢ѹǿ5.05��104 Pa | D���¶�0�桢ѹǿ5.05��104 Pa |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�����ܱ������������淴Ӧ

 ����
���� ʱ�̷�Ӧ�ﵽƽ�⣬��
ʱ�̷�Ӧ�ﵽƽ�⣬�� ʱ����С���������
ʱ����С���������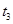 ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
| A��Z��W�ڸ�������������һ����Ϊ��̬ |
B�� ʱ����� ʱ�����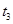 ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ��������������� ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ��������������� |
C�����ڸ��¶��´˷�Ӧƽ�ⳣ������ʽΪK=c��X������ ʱ����� ʱ�����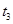 ʱ�̺��XŨ�Ȳ���� ʱ�̺��XŨ�Ȳ���� |
D�����÷�Ӧֻ��ij�¶� �����Է����У���÷�Ӧ��ƽ�ⳣK���¶����߶����� �����Է����У���÷�Ӧ��ƽ�ⳣK���¶����߶����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ĸ���ͬ�������н��кϳɰ��ķ�Ӧ��������������ͬʱ���ڲⶨ�Ľ�����ж����ɰ�������������
| A��v (N2)=0��05mol��L��1��s��1 | B��v (H2)=0��3mol��L��1��min��1 |
| C��v (N2)=0��2 mol��L��1��min��1 | D��v (NH3)=0��3 mol��L��1��min��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
CO��g��+H2O��g�� H2��g��+CO2��g����H��0����������������������,˵����ȷ���� �� ��
H2��g��+CO2��g����H��0����������������������,˵����ȷ���� �� ��
| A������������ı��˷�Ӧ��;������Ӧ�ġ�HҲ��֮�ı� |
| B���ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų����������� |
| C�������¶ȣ���Ӧ���ʼӿ죬��Ӧ�ų����������� |
| D������ԭ����н��У���Ӧ�ų����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�¶��£����һ�����ܱ������н��п��淴Ӧ��X(g)��Y(g) Z(g)��W(s) ��H > 0��
Z(g)��W(s) ��H > 0��
����������ȷ����
| A����������W���淴Ӧ�������� |
| B���������������ܶȲ���ʱ����Ӧ�ﵽƽ�� |
| C�������¶ȣ�Y�İٷֺ������� |
| D��ƽ������X��������Ӧ�Ħ�H���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���¡����ݵ������¶���N2(g)��3H2(g) 2NH3(g)����H��0�ķ�Ӧ���ﵽ��ѧƽ��״̬�ı�־Ϊ(�� )
2NH3(g)����H��0�ķ�Ӧ���ﵽ��ѧƽ��״̬�ı�־Ϊ(�� )
| A���Ͽ�һ��N��N����ͬʱ��6��N��H������ |
| B�����������ܶȲ��� |
| C����������ѹǿ���� |
| D��N2��H2��NH3������֮��Ϊ1��3 ��2��״̬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com