
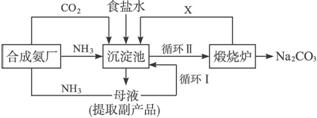

图6-20
(1)上述生产纯碱的方法称_____________,副产品的一种用途为_____________。
(2)沉淀池中发生的化学反应方程式是_____________。
(3)写出上述流程中X物质的化学式_____________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了_____________(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是_____________。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加_____________。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气的作用有_____________。
a.增大![]() 的浓度,使NH4Cl更多地析出
的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
解析:本题主要考查侯德榜制碱法的生产原理及生产工艺、Cl-的检验等,根据联合制碱法的生产原理,可知向食盐水中通入氨气是为了得到碱性溶液,以吸收更多的CO2,当CO2过量时发生反应:NH3+CO2+H2O====NH4HCO3 NH4HCO3+NaCl====NaHCO3↓+NH4Cl,当NaHCO3在煅烧炉中受热时分解:2NaHCO3![]() Na2CO3+CO2↑+H2O,故X为CO2。要提高NaCl的利用率,必须将过滤出NaHCO3的母液循环利用。要检验Na2CO3中是否混有NaCl,只需向其溶液中加入硝酸酸化的AgNO3溶液看是否有白色沉淀即可。在向母液中通入NH3时发生反应
Na2CO3+CO2↑+H2O,故X为CO2。要提高NaCl的利用率,必须将过滤出NaHCO3的母液循环利用。要检验Na2CO3中是否混有NaCl,只需向其溶液中加入硝酸酸化的AgNO3溶液看是否有白色沉淀即可。在向母液中通入NH3时发生反应![]() +NH3====
+NH3====![]() +
+![]() ,c(
,c(![]() )增大,NaHCO3转化为Na2CO3。
)增大,NaHCO3转化为Na2CO3。
答案:(1)联合制碱法或侯德榜制碱法 化肥或电解液或焊药等
(2)NH3+CO2+H2O+NaCl====NH4Cl+NaHCO3↓
或NH3+CO2+H2O====NH4HCO3 NH4HCO3+NaCl====NaHCO3↓+NH4Cl
(3)CO2 (4)Ⅰ 过滤 (5)稀硝酸和硝酸银溶液 (6)a、c


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| ||
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com