
| A. | H+、Na+、OH- | B. | Na+、NO3-、Cl- | ||
| C. | K+、H+、HCO3- | D. | Ca2+、SO42-、CO32- |
科目:高中化学 来源: 题型:选择题
| A. | NaNO2是还原剂 | |
| B. | NH4Cl中N元素被还原 | |
| C. | 生成1 mol N2时转移6 mol电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
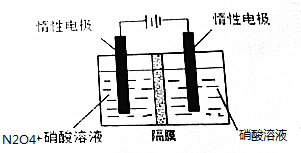
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 用二氧化碳制全降解塑料,可以缓解温室效应 | |
| C. | 氧化铝陶瓷和光导纤维都属于无机非金属材料 | |
| D. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO 2分子比例模型: | B. | S 2-的结构示意图: | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | D. | HCN分子的结构式:H-C≡N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L KNO3溶液:、H+、Fe2+、Al3+、Cl- | |
| B. | 酸性溶液:NH4+、Fe2+、K+、SO42- | |
| C. | 碱性溶液:ClO-、SO32-、K+、Na+ | |
| D. | 与铝反应产生大量氢气的溶液:K+、Cl-、CO32-、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com