
下列实验没有错误的是( )
A. 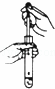
向试管中滴加液体 B. 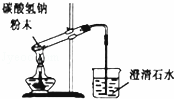
碳酸氢钠受热分解
C. 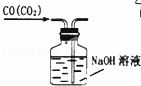
除去CO气体中的CO2气体 D. 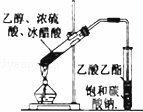
乙酸乙酯的制备
考点: 化学实验方案的评价.
分析: A.向试管中滴加液体,胶头滴管不能深入到试管中;
B.给固体加热时,试管口应该稍稍向下倾斜;
C.洗气装置中的导管应该采用长进短出;
D.根据实验室制取乙酸乙酯的反应原理及装置进行判断.
解答: 解:A.胶头滴管深入到试管中,容易污染试剂,所以胶头滴管不能深入到试管中,故A错误;
B.给碳酸氢钠加热时,导管口应该稍稍向下倾斜,避免碳酸氢钠分解生成的水进入试管,导致试管炸裂,故B错误;
C.洗气瓶中导管应该采用长导管进气,短导管出气的方法,否则成了排水法收集气体装置,故C错误;
D.实验室制取乙酸乙酯,试管中的试剂为乙酸、乙醇、浓硫酸,吸收试剂为饱和碳酸钠溶液,该实验装置正确,样品合理,故D正确;
故选D.
点评: 本题考查了样品的取用、乙酸乙酯的制取、物质的分离与提纯等操作方法判断,题目难度不大,注意掌握实验室中基本的实验操作方法,能够对错误操作作出正确判断.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂.工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣=2FeO42﹣+3Cl﹣+5H2O,
干法制备的主要反应方程为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
则下列有关说法正确的是()
A. 高铁酸钾中铁显+6价
B. 湿法中FeO42﹣是还原产物
C. 干法中每生成1mol Na2FeO4 转移4mol电子
D. K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,可以说明金属甲比乙活泼性强的是()
A. 将甲乙作电极组成原电池时甲是负极
B. 甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲上有H2气放出
C. 在氧化还原反应中,甲比乙失去的电子多
D. 同价态的阳离子,甲比乙的氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或对实验事实的叙述中,正确的是( )
A. 用氨气做喷泉实验主要是利用氨气的水溶液呈碱性这一性质
B. 向浓硫酸中缓慢加蒸馏水,以稀释浓硫酸
C. 常温下,浓硝酸可贮存于铁制或铝制容器中
D. 向溶液中加入硝酸酸化的BaCl2溶液,产生白色沉淀,说明一定含有SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
硅及其化合物在材料领域中应用广泛.下列叙述中不正确的是( )
A. 硅单质可用来制造太阳能电池
B. 装碱性溶液的玻璃试剂瓶不能用玻璃塞
C. 二氧化硅是制造光导纤维的材料
D. 二氧化硅属于酸性氧化物,不能与任何酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是( )
A. 氧化亚铁和稀硝酸反应FeO+2H+═Fe2++H2O
B. 硫酸铝溶液与足量烧碱:Al3++3OH﹣=Al(OH)3↓
C. 氯化亚铁溶液中滴入氯水Cl2+2Fe2+═2Cl﹣+2Fe3+
D. 金属铝投入NaOH溶液中2Al+2OH﹣+2H2O═2AlO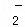 +2H2↑
+2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
今有如下三个热化学方程式:
H2(g)+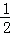 O2(g)═H2O(g)△H=a kJ•mol﹣1
O2(g)═H2O(g)△H=a kJ•mol﹣1
H2(g)+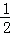 O2(g)═H2O(l)△H=b kJ•mol﹣1
O2(g)═H2O(l)△H=b kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l)△H=c kJ•mol﹣1
关于它们的下列表述正确的是()
A. 它们都是吸热反应 B. a、b和c均为正值
C. a=b D. 2b=c
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值.下列说法正确的是()
A. 1 mol甲苯含有C﹣H键数目为8NA
B. 1 mol丙烯酸中含有双键的数目为NA
C. 由a g C2H4和C3H6组成的混合物中所含共用电子对数目为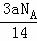
D. 在过氧化钠跟水的反应中,每生成2.24 L氧气,转移电子的数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com