
| A. | 1NA个氢气分子所占的体积为22.4 L | |
| B. | 2NA个二氧化碳分子的质量为88 g | |
| C. | 0.1 mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| D. | 17 g NH3中所含原子数为NA |
分析 A、氢气所处的状态不明确;
B、求出二氧化碳的物质的量,然后根据质量=nM;
C、溶液体积不明确;
D、求出氨气的物质的量,然后根据氨气中含4个原子来分析.
解答 解:A、氢气所处的状态不明确,故所占的体积无法计算,故A错误;
B、2NA个二氧化碳的物质的量为2mol,而质量=nM=2mol×44g/mol=88g,故B正确;
C、溶液体积不明确,故溶液中的离子个数无法计算,故C错误;
D、17g氨气的物质的量为1mol,而氨气中含4个原子,故1mol氨气中含4NA个原子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、Ca2+、HCO3-、Cl- | B. | Cu2+、Na+、NO3-、Cl- | ||
| C. | Na+、K+、Mg2+、SO42- | D. | Mg2+、Fe3+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水电离方程式为:NH3•H2O=NH4++OH- | |
| B. | 溶液中有:c(NH4+)+c(H+)=c(OH-) | |
| C. | 溶液中:c(NH3•H2O)=0.1mol/L | |
| D. | 加入少量NaOH固体,溶液中碱性增强,c(H+)•c(OH-)的乘积将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
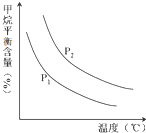 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法正确的是( )| A. | 对应简单离子半径:Z>X>W | |
| B. | 对应气态氢化物的稳定性Y>Z | |
| C. | 化合物XZW既含离子键,又含共价键 | |
| D. | Y的氧化物既能与Z的氢化物溶液反应,又能与X的最高价氧化物对应水化物的溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液质量减轻 | |
| B. | Fe3+的氧化性大于Cu2+ | |
| C. | 溶液中Cu2+与Fe2+的物质的量比为1:1 | |
| D. | 1 mol Fe可还原2 mol Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
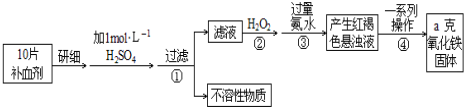
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
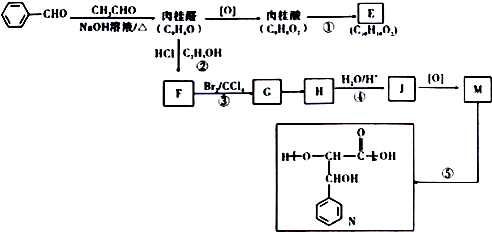
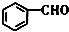 的名称是苯甲醛.
的名称是苯甲醛.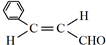 ,分子中最多有18个原子共平面.
,分子中最多有18个原子共平面. .
.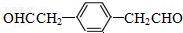 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com