
【题目】25℃时,将体积为Va、pH=a的某一元酸与体积Vb、pH=b的某一元碱混合,请完成下列各题.
(1)若a+b=14,2Va=Vb , 碱是NaOH,反应后所得溶液pH小于7.由此你能得到的结论是 .
(2)若a+b=13,酸是盐酸,碱是b=12的KOH,现用盐酸滴定50.00mL KOH溶液,当滴定到溶液的pH=2时,消耗盐酸的体积V=mL.
(3)若已知Va<Vb和a=0.5b,酸是强酸,碱是强碱,酸和碱恰好中和,则a的取值范围是 .
【答案】
(1)酸是一种弱酸
(2)11.11
(3)![]() <a<
<a< ![]()
【解析】解:(1)解:pH=a的酸的溶液中c(H+)=10﹣pH molL﹣1=10﹣amolL﹣1 , a+b=14,则pH=b的碱中c(OH﹣)=10pH﹣14 molL﹣1=10b﹣14 molL﹣1=10﹣amolL﹣1 , 可见酸中c(H+)与碱中c(OH﹣)相等,2Va=Vb混合后溶液的pH小于7,说明溶液呈酸性,应为弱酸与强碱的组合,所以答案是:酸是一种弱酸;(2)酸中c(H+)=10﹣pH molL﹣1=10﹣amolL﹣1 , 碱中c(OH﹣)=10pH﹣14 molL﹣1=10b﹣14 molL﹣1=10﹣(a+1)molL﹣1 , pH=2时,c(H+)=10﹣2mol/L= ![]() ,解得:V=0.0111L=11.11mL,所以答案是:11.11;(3)pH=b的某一元强碱溶液呈碱性,则b>7, a=0.5b,则a>0.5×7=3.5,即a>
,解得:V=0.0111L=11.11mL,所以答案是:11.11;(3)pH=b的某一元强碱溶液呈碱性,则b>7, a=0.5b,则a>0.5×7=3.5,即a> ![]() ; pH=a的强酸c(H+)=10﹣amol/L,pH=b的强碱c(OH﹣)=10b﹣14mol/L,恰好中和,则有Va×10﹣a=Vb×10b﹣14 , 可得:
; pH=a的强酸c(H+)=10﹣amol/L,pH=b的强碱c(OH﹣)=10b﹣14mol/L,恰好中和,则有Va×10﹣a=Vb×10b﹣14 , 可得: ![]() =10a+b﹣14 , Va<Vb,则10a+b﹣14<1,即:a+b<14,又a=0.5b,则a+2a<14, 3a<14,则a<
=10a+b﹣14 , Va<Vb,则10a+b﹣14<1,即:a+b<14,又a=0.5b,则a+2a<14, 3a<14,则a< ![]() ,所以:
,所以: ![]() <a<
<a< ![]() ,所以答案是:
,所以答案是: ![]() <a<
<a< ![]() .
.


科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA
B.标准状况下,44.8LNO与22.4LO2混合后气体中分子总数等于2NA
C.NO2和H2O反应每生成2molHNO3时转移的电子数目为2NA
D.lmolFe在氧气中充分燃烧失去3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下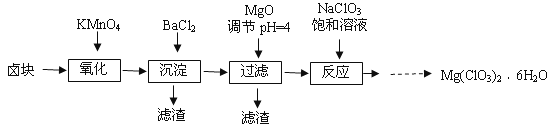
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
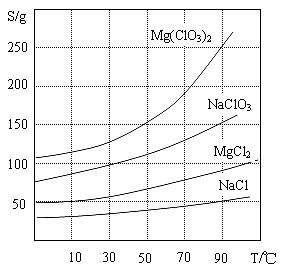
(1)过滤所需要的主要玻璃仪器有 ,
(2)加入BaCl2的目的是 ,加MgO后过滤所得滤渣的主要成分为 。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为 ,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①蒸发结晶;② ;洗涤;③将滤液冷却结晶;④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:(已知Mg(ClO3)2·6H2O的摩尔质量为299g/mol)
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7 溶液滴定剩余的Fe2+至终点。反应的方程式为: Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7 溶液15.00 mL。
①写出步骤2中发生反应的离子方程式: ;
② 产品中Mg(ClO3)2·6H2O的质量分数为 。(保留到小数点后一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2PbCl4溶液,生成Pb,装置如下图,下列说法不正确的是
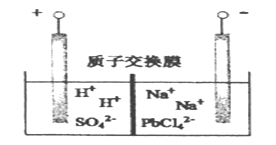
A. 阴极的电极反应式为 PbCl42- +2e- =Pb + 4Cl-
B. 电解一段时间后,Na2PbCl4浓度极大下降,可加入PbO恢复其浓度
C. 电解过程中阳极溶液的pH减小,阴极的pH保持不变
D. 电路中通过0.2mol,则阴极的质量增加20.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.分子式为C2H6O的有机化合物性质相同
B.相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能途径a:C ![]() CO+H2
CO+H2 ![]() CO2+H2O
CO2+H2O
途径b:C ![]() CO2
CO2
C.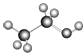 可以表示乙醇分子的球棍模型
可以表示乙醇分子的球棍模型
D.![]() :既可以表示甲烷分子,也可以表示四氯化碳分子
:既可以表示甲烷分子,也可以表示四氯化碳分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:
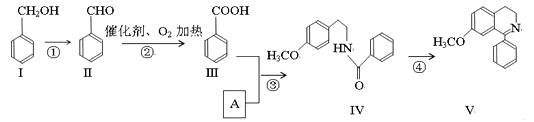
(1)写出Ⅳ中含氧官能团的名称_____________________。
(2)写出Ⅳ物质的分子式_____________。
(3)写出下列反应的类型②___________,③________________。
(4)反应②的化学方程式___________________________________。
(5)Ⅰ和Ⅲ在浓硫酸催化加热时反应的化学方程式__________________________。
(6)A的结构简式_______________________。
(7)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种。写出满足上述条件的Ⅵ的结构简式________________________。
(8)一定条件下,化合物Ⅶ(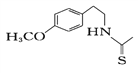 )也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式__________________________________。
)也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com