
【题目】常温下,分别向NaA溶液和MCl溶液中加入盐酸和NaOH溶液,混合溶液的pH与离子浓度变化关系如下图所示.下列说法不正确的是( )

A. 曲线L1表示![]() 与pH的变化关系
与pH的变化关系
B. Ka(HA)=1×10-5.5
C. a点时两溶液中水的电离程度相同
D. 0.10mol/L MA溶液中存在:c(M+)>c(A-)>c(OH-)>c(H+)
【答案】C
【解析】
A.MCl溶液中加入NaOH溶液,溶液的pH逐渐增大,M+离子逐渐减小,MOH的浓度逐渐增大,则lg![]() 的值逐渐减小,则曲线L1表示lg
的值逐渐减小,则曲线L1表示lg![]() 与pH的变化关系,故A正确;
与pH的变化关系,故A正确;
B.曲线L2表示lg![]() 与pH的变化关系,lg
与pH的变化关系,lg![]() =0时,
=0时,![]() =1,此时pH=5.5,c(H+)=1×10-5.5mol/L,则Ka(HA)=
=1,此时pH=5.5,c(H+)=1×10-5.5mol/L,则Ka(HA)=![]() = c(H+)=1×10-5.5,故B正确;
= c(H+)=1×10-5.5,故B正确;
C.a点溶液的pH>7,对于曲线L2,由于A-离子水解导致溶液呈碱性,促进了水的电离,而对于曲线L1,MCl溶液呈酸性,a点时呈碱性,说明MOH的电离程度大于M+离子水解程度,抑制了水的电离,所以两溶液中水的电离程度不同,故C错误;
D.曲线L1中,lg![]() =0时,
=0时,![]() =1,Kb(MOH)=c(OH-)>1×10-5>1×10-5.5,根据Kh=
=1,Kb(MOH)=c(OH-)>1×10-5>1×10-5.5,根据Kh=![]() 可知,电离平衡常数越大,对应离子的水解程度越小,则水解程度A->M+,则MA溶液呈碱性,则c(OH-)>c(H+)、c(M+)>c(A-),溶液中离子浓度大小为:c(M+)>c(A-)>c(OH-)>c(H+),故D正确。
可知,电离平衡常数越大,对应离子的水解程度越小,则水解程度A->M+,则MA溶液呈碱性,则c(OH-)>c(H+)、c(M+)>c(A-),溶液中离子浓度大小为:c(M+)>c(A-)>c(OH-)>c(H+),故D正确。
故选C。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】I.含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
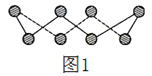
(1)S单质的常见形式为S8,其环状结构如图1所示,S原子采用的轨道杂化方式是_____。
(2)H2SeO4比H2SeO3酸性强的原因:_________。
(3)ZnS在光导体材料、荧光体、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图2所示,其晶胞边长为a pm,密度为______gcm3。(用含a和NA的表达式填空)

II.氮及其化合物与人类生产、生活息息相关。化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44+,N4H44+遇到碱性溶液会生成一种形似白磷(P4)的N4分子。请回答下列问题:
(4)N4分子中的氮氮键的键角为____,1molN4分子中含有的氮氮键的数目为____。
(5)N4比P4的沸点____(填“高”或“低”),原因为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置确认该混合气体中是否含有SO2和C2H4。请回答下列问题:
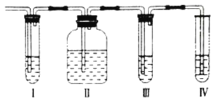
⑴上述Ⅰ、Ⅳ装置可盛放的试剂是:Ⅰ____;Ⅳ___;(请将下列有关试剂的序号填入对应装置内,可重复选用)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
⑵能说明SO2气体存在的现象是________
⑶使用装置Ⅱ的目的是_______;有关反应的离子方程式是_____。
⑷确定含有乙烯的现象是_______。
⑸为了制备重要的有机原料氯乙烷(CH3CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备;
乙同学:选乙烯和适量HCl在一定条件下制备。
你认为上述两位同学的方案中,合理的是______的方案。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )
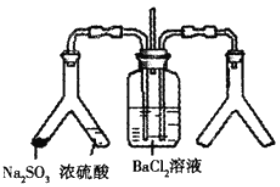
A. Cu和浓硝酸 B. CaO和浓氨水
C. 大理石和稀盐酸 D. 高锰酸钾溶液和浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的方向和限度的说法中正确的是( )
A. mA(g)+nB(g)![]() pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p
pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p
B. 将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s) ![]() 2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据
2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据
C. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0
D. 对于反应A(g)+B(g)![]() 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变
2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于非氧化还原反应的是
A. 2Mg+CO2![]() 2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
C. SO2+H2O2=H2SO4D. Br2+2NaI=2NaBr+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图___,R的简单离子的电子式___。
②X与Y元素可形成一种常用的消毒剂,其结构式为__。
③Y、Z、W、R形成的简单离子半径由大到小顺序为___(用化学符号表示)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置___。
②关于铷的下列说法中不正确的是___(填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
![]()
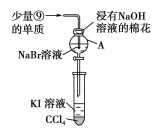
①棉花中浸有NaOH溶液的作用是___(用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到___;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F的核电荷数依次增大,且均为核电荷数小于18的非稀有气体元素。A的单质是自然界中密度最小的气体,A和C可形成A2C和A2C2两种常见的液态化合物,B、C原子的最外层电子数之和等于11,D+与C的简单离子的核外电子排布相同,C、E原子的最外层电子数相同。请回答下列问题:
(1)写出元素符号:B__,D__。
(2)A元素具有两个中子的核素的表示符号为__,E的简单离子的结构示意图是__。
(3)A2C2的分子式为__。
(4)将少量F的单质通入足量NaOH溶液中,发生反应的离子方程式是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com