
分析 (1)根据物质的组成和性质判断:CaO是金属氧化物,其它是非金属氧化物;铜与酸不反应,其它金属都能与盐酸反应产生氢气;
(2)化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;
分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”;
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应;
复分解反应是两种化合物相互交换成分生成两种新的化合物的反应;
有化合价变化的反应属于氧化还原反应.
解答 解:(1)CaO是金属氧化物,其它是非金属氧化物;铜与酸不反应,其它金属都能与盐酸反应产生氢气,故答案为:CaO;Cu;
(2)A.2Na+2H2O═2NaOH+H2↑,属于置换反应;
B.CH4+2O2→CO2+2H2O,不属于四种基本反应类型;
C.2KClO3═2KCl+3O2↑,属于分解反应;
D.CaCO3+2HCl═CaCl2+H2O+CO2↑,属于复分解反应;
E.Na2O+CO2═Na2CO3 属于化合反应;
F.CO2+C═2CO属于化合反应;
A.2Na+2H2O═2NaOH+H2↑,B.CH4+2O2→CO2+2H2O,C.2KClO3═2KCl+3O2↑,F.CO2+C═2CO都有化合价的变化,属于氧化还原反应;
故答案为:EF;C;D;A;ABCF.
点评 本题考查了化学的基本概念和反应类型的判断,熟悉概念的内涵和外延是解题关键,注意分析氧化还原反应,应抓住化合价的变化,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
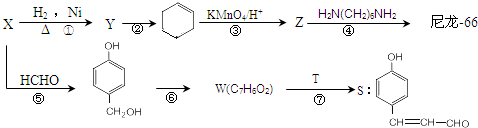
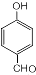 ,T的分子式为C2H4O.
,T的分子式为C2H4O.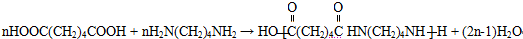 .
.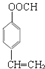 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
| 步骤2:取适量滤液于试管中,滴加稀硫酸. | |
| 步骤3:取适量步骤1中的沉淀于试管中,取适量步骤1中的沉淀于试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中. | |
| 步骤4:取适量滤液于烧杯中,用pH计测其 pH值 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 1molCu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 18gD2O和18gH2O中含有的质子数均为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 75 mL 1.5 mol•L-1氯化钾溶液 | ||
| C. | 150 mL 3 mol•L-1氯化钾溶液 | D. | 50 mL 3 mol•L-1氯化镁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:相关数据如下:
实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:相关数据如下:| 相对分子质量 | 密度/(g•cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com