
| A. | 2CO+O2═2CO2 | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | 2KClO3═2KCl+3O2↑ | D. | Fe2O3+3CO═2Fe+3CO2 |
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质量数不同,属于两种元素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、H2互为同位素 | |
| C. | 14462Sm其原子核内中子数和质子数都是62 | |
| D. | O2和O3互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应△H1>△H2 | |
| B. | 由C(石墨)→C(金刚石)△H=+1.9kJ/mol,可知金刚石比石墨稳定 | |
| C. | 已知在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量.则有关氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=+285.8kJ/mol | |
| D. | 在稀溶液中,H+ (aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol硫酸的浓硫酸与含1 molNaOH的溶液混合,放出的热量大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
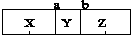 ),下列说法中错误的是( )
),下列说法中错误的是( )| A. | 若Y是C4H8,则X可能是N2 | B. | 分子数目:X=Z=2Y | ||
| C. | 若X是O2,则Z不可能是CO2 | D. | 气体密度:X=Z=2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25 mL 0.2mol/L的NaCl溶液 | B. | 100mL 0.1 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
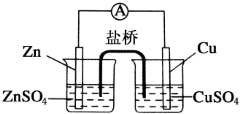
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
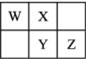 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A. | Y元素氧化物对应水化物的酸性一定弱于Z | |
| B. | W、X、Y中最简单氢化物稳定性最强的是X | |
| C. | X元素形成的单核阴离子还原性大于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com