
【题目】化合物M可用于消毒剂、抗氧化剂、医药中间体。实验室由芳香烃A制备M的一种合成路线如下:

请回答:
(1)B的化学名称为___________;D中官能团的名称为______________________。
(2)由F生成G的反应类型为___________;F的分子式为___________。
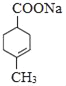
(3)由E转化为F的第一步反应的化学方程式为______________________。
(4)M的结构简式为___________。
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式______________________。
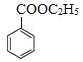
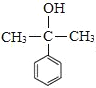
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备 的合成路线_________________________________。
的合成路线_________________________________。
【答案】对甲基苯甲醛(或4﹣甲基苯甲醛) 羧基、氯原子 酯化反应或取代反应 C8H12O2 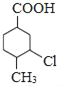 +2NaOH
+2NaOH![]()
 +NaCl+2H2O
+NaCl+2H2O 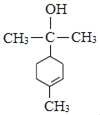
![]() 或
或![]() ;
; 
![]()
![]()
![]()
【解析】
A的分子式为C7H8,结合B的结构,应是A与CO发生加成反应生成B(对甲基苯甲醛),可知A为![]() 。对比B与C的结构,结合反应条件、C的分子式,可知B中醛基氧化为羧基得到C,C与氯气发生苯环上取代反应生成D,D与氢气发生加成反应生成E,E发生取代反应生成F,故C为
。对比B与C的结构,结合反应条件、C的分子式,可知B中醛基氧化为羧基得到C,C与氯气发生苯环上取代反应生成D,D与氢气发生加成反应生成E,E发生取代反应生成F,故C为![]() 、D为
、D为![]() 、E为
、E为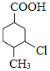 。F与乙醇发生酯化反应生成G为
。F与乙醇发生酯化反应生成G为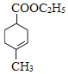 ,G发生信息中反应生成M为
,G发生信息中反应生成M为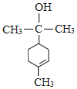 ,据此分析解答。
,据此分析解答。
(1)B的结构简式为![]() ,名称为对甲基苯甲醛(或4﹣甲基苯甲醛);D为
,名称为对甲基苯甲醛(或4﹣甲基苯甲醛);D为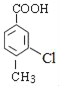 ,其中 官能团有羧基、氯原子,故答案为:对甲基苯甲醛(或4﹣甲基苯甲醛);羧基、氯原子;
,其中 官能团有羧基、氯原子,故答案为:对甲基苯甲醛(或4﹣甲基苯甲醛);羧基、氯原子;
(2)由F生成G发生酯化反应,也属于取代反应;F的分子式为C8H12O2,故答案为:酯化反应或取代反应;C8H12O2;
(3)由E转化为/span>F的第一步反应的化学方程式为: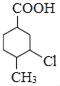 +2NaOH
+2NaOH![]()
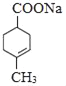 +NaCl+2H2O,故答案为:
+NaCl+2H2O,故答案为: +2NaOH
+2NaOH![]()
 +NaCl+2H2O;
+NaCl+2H2O;
(4)由分析可知M的结构简式为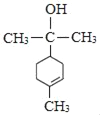 ,故答案为:
,故答案为: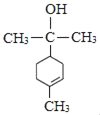 ;
;
(5)芳香化合物Q为C(![]() )的同分异构体,Q能发生银镜反应,说明含有醛基或甲酸形成的酯基,其核磁共振氢谱有4组吸收峰。符合要求的Q的结构简式为:
)的同分异构体,Q能发生银镜反应,说明含有醛基或甲酸形成的酯基,其核磁共振氢谱有4组吸收峰。符合要求的Q的结构简式为:![]() 、
、![]() ,故答案为:
,故答案为:![]() 或
或![]() ;
;
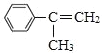
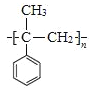
(6) 加聚反应得到
加聚反应得到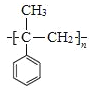 ,
,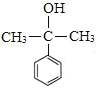 发生消去反应得到
发生消去反应得到 ,由信息可知苯甲酸乙酯与①CH3MgBr、②H+/H2O作用得到
,由信息可知苯甲酸乙酯与①CH3MgBr、②H+/H2O作用得到 ,合成路线流程图为
,合成路线流程图为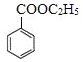
![]()

![]()

![]()
 ,故答案为:
,故答案为:
![]()

![]()

![]()
 。
。


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】科学家将水置于足够强的电场中,在20℃时水分子瞬间凝固可形成“暖冰”。某兴趣小组做如图所示实验,发现烧杯中酸性KMnO4溶液褪色,且有气泡产生。将酸性KMnO4溶液换成FeCl3溶液,烧杯中溶液颜色无变化,但有气泡产生。则下列说法中正确的是( )

A. 20℃时,水凝固形成的“暖冰”所发生的变化是化学变化
B. “暖冰”是水置于足够强的电场中形成的混合物
C. 烧杯中液体为FeCl3溶液时,产生的气体为Cl2
D. 该条件下H2燃烧的产物中可能含有一定量的H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-=![]() +4H2O
+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用CH3COOD与CH3CH2OH在浓硫酸作用下发生酯化反应,一段时间后分子中存在D原子的是( )
①乙酸,②乙醇, ③乙酸乙酯,④水
A. ①④B. ①③④C. ①②③④D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①装置D的名称为___________。
②按照气流从左到右的方向,上述装置的连接顺序为___________→尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间N2,其目的为______________________。
④实验证明了气体产物中含有CO,依据的实验现象为______________________。
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___________。
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为___________。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol· L -1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为____________________________________________。
(5)草酸亚铁晶体样品的纯度为____________________________________________;若步骤1配制溶液时部分Fe2+被氧化,则测定结果将___________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,将agNH3完全溶于水,得到VmL溶液,设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为bmol。下列叙述中不正确的是
A.溶质的质量分数ω=![]() ×100%
×100%
B.溶质的物质的量浓度c=1000a/17Vmol·L-1
C.溶液中c(OH-)=1000b/Vmol·L-1+c(H+)
D.上述溶液中再加入VmL水后,所得溶液中溶质的质量分数小于0.5ω
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列有关说法不正确的是

A. 右侧电极反应方程式:Fe+8OH--6e-=FeO42-+4H2O
B. 左侧为阳离子交换膜,当Cu电极生成1mol气体时,有2molNa+通过阳离子交换膜
C. 可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作
D. Na2FeO4具有强氧化性且产物为Fe3+,因此可以利用Na2FeO4除去水中的细菌、固体颗粒以及Ca2+等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com