
分析 (1)依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积,依据浓硫酸体积选择合适规格量筒;
(2)配制一定物质的量浓度溶液一般步骤为:计算、量取、稀释、移液、洗涤、定容、摇匀等,据此选择需要仪器;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解:(1)用18mol•L-1 浓硫酸配制80mL 3.0mol•L-1 稀硫酸,应选择100mL容量瓶,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18mol/L×V=100mL×3.0mol/L,解得V=16.7mL,应选择25mL量筒;
故答案为:16.7mL;B;
(2)配制一定物质的量浓度溶液一般步骤为:计算、量取、稀释、移液、洗涤、定容、摇匀等,用到的仪器:量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,所以还缺少的玻璃仪器:100mL容量瓶、胶头滴管;
故答案为:100mL容量瓶、胶头滴管;
(3)a.容量瓶没有干燥,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故a不选;
b.摇匀后观察发现溶液未达刻度线,再用滴管加几滴蒸馏水至刻度线,导致溶液体积偏大,溶液浓度偏小,故b选;
c.定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故c不选;
d.溶液具有均一性,摇匀后,取溶液时不慎将溶液溅出对溶液浓度不产生影响,故c不选;
e.用量筒量取浓硫酸后未用蒸馏水将量筒洗涤2-3次,导致量取浓硫酸中含有硫酸的物质的量偏小,溶液浓度偏小,故e选;
故选:be.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,难度不大,掌握公式的运用和配制原理是解题的关键,注意误差分析的方法和技巧.


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:选择题
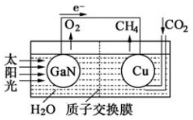 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )| A. | 氮化镓是一种新型无机非金属材料 | |
| B. | 铜电极表面的电极反应式:CO2+8H++8e-═CH4+2H2O | |
| C. | 溶液中H+穿过质子交换膜从左向右移动 | |
| D. | 为提高该人工光合系统的工作效率,可向装置中加入少量硫酸或盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
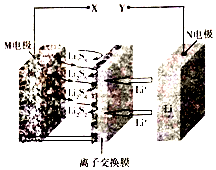 新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )
新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )| A. | 电池充电时X为电源负极 | |
| B. | 放电时,正极上可发生反应:2Li++Li2S4+2e-=2Li2S2 | |
| C. | 充电时,每生成1molS8转移0.2mol电子 | |
| D. | 离子交换膜只能通过阳离子,并防止电子通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度 n(CO) 时间 | 0 | 10 | 20 | … | 40 | 50 |
| T1 | 1.0 | 0.7 | 0.5 | … | 0.25 | 0.25 |
| T2 | 1.0 | 0.65 | 0.4 | … | 0.28 | 0.28 |
| A. | T1温度下平衡后恒容再充入0.5molCO,重新平衡后CO总的转化率与H2相等 | |
| B. | T1温度下10-20sH2的反应速率为0.04mol•L-1•s-1 | |
| C. | 该反应的△Η>0 | |
| D. | T2温度下平衡后恒定压强不变充入0.28molCH3OH,CH3OH的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 5:1 | C. | 7:2 | D. | 8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与浓硫酸共热消去 | B. | 与浓氢溴酸卤代 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 导电性强的溶液一定是强电解质溶液 | |
| B. | H2SO4是强电解质,稀硫酸中没有H2SO4分子 | |
| C. | NaCl晶体是由Na+和Cl-组成,NaCl晶体是良导体 | |
| D. | 氯气和氨气的水溶液导电性都很好,所以它们是强电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com